题目内容
12.现由60袋碳酸钠,欲配制成15%的碳酸钠溶液需加入多少m3的水?按碱槽现有容积24m3来看,可否一次性配制完60袋碳酸钠?(杂质不计,50kg/袋,碱槽充装系数为0.8)分析 据w=$\frac{{m}_{质}}{{m}_{质}+{m}_{液}}×100%$进行计算m液的质量,并求其水的体积;若求算溶液的体积>碱槽充装,则不能一次性配制,反之能.
解答 解:w=$\frac{{m}_{质}}{{m}_{质}+{m}_{液}}×100%$
则:15%═$\frac{60袋×50kg/袋}{60袋×50kg/袋+{m}_{液}}$×100%,解得m液=17000Kg,V水=$\frac{17000kg}{1000kg/{m}^{3}}$=17m3,
答:欲配制成15%的碳酸钠溶液需加入17m3的水.
碱槽充装系数为0.8,故24m3碱槽则只能充装0.8×24m3=19.2m3的液体,17m3<19.2m3故能一次性配制完60袋碳酸钠,
答:能一次性配制完60袋碳酸钠.
点评 准确运用w=$\frac{{m}_{质}}{{m}_{质}+{m}_{液}}×100%$此公式是本题解题的关键,本题难度中等.

练习册系列答案
相关题目
2.下列关于容量瓶的相关叙述中正确的是( )
| A. | 容量瓶上标有:①浓度、②容量、③刻度线 | |
| B. | 使用容量瓶前应先检查它是否漏水 | |
| C. | 容量瓶先用蒸馏水洗净,再用待配液润洗 | |
| D. | 氢氧化钠溶解后可马上转移到容量瓶中 |
3.除去下列溶液中的杂质(括号内为杂质),选择试剂不正确的是( )
| A. | CO2(HCl)--用饱和NaHCO3溶液 | B. | NaOH(Ba(OH)2)--用Na2SO4溶液 | ||
| C. | NaCl(Na2SO4)--用Ba(NO3)2溶液 | D. | Na2CO3(NaHCO3)--用NaOH溶液 |
20.在常温下,将pH=9的NaOH溶液与pH=11的NaOH溶液等体积混合后,溶液的pH最接近于( )
| A. | 9.3 | B. | 9.7 | C. | 10 | D. | 10.7 |
7.下列说法正确的是( )
| A. | 离子化合物中只能含有离子键 | |
| B. | 化学反应的过程,本质上是旧化学键断裂和新化学键形成的过程 | |
| C. | 化学键存在于分子之间 | |
| D. | 共价化合物中可能含有离子键 |
4.下列图示与对应的叙述相符的是( )
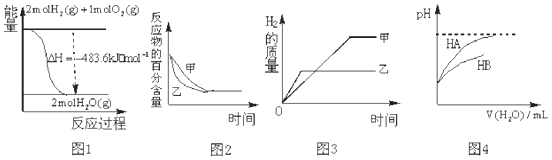

| A. | 图 1 表示 H2与O2发生反应过程中的能量变化,则H2的燃烧热为 241.8kJ•mol-1 | |
| B. | 图 2 表示压强对可逆反应 2A(g)+2B (g)?3C(g)+D(s)的影响,乙的压强比甲的压强大 | |
| C. | 图 3 表示等质量的钾、钠分别与足量水反应,则甲为钠 | |
| D. | 图 4 表示常温下,稀释 HA、HB 两种酸的稀溶液时,溶液 pH 随加水量的变化,则相同条件下 NaA溶液的 pH 大于同浓度的 NaB 溶液的 pH. |
7.下列有关图示与对应的叙述正确的是( )
| A. | 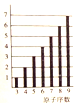 图纵坐标为元素的最高正价 | |
| B. |  图可说明反应2NO+2CO=N2+2CO2为吸热反应 | |
| C. | 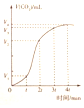 若图表示的是一定量的CaCO3与盐酸反应生成CO2的体积随时间的变化,则t~2tmin反应速率最快 | |
| D. | 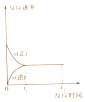 若图表示的是反应N2(g)+3H2(g)?2NH3(g)的.v(正)、v(逆)随时间的变化,则0~t1时间段:v(正)=v(逆) |
8.水杨酸、冬青油、阿司匹林的结构简式如图,下列说法不正确的是( )
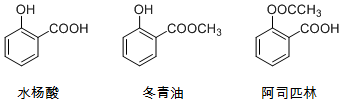

| A. | 由水杨酸制冬青油的反应是取代反应 | |
| B. | 阿司匹林的分子式为C9H8O4,水解可得水杨酸 | |
| C. | 冬青油苯环上的一氯取代物有4种 | |
| D. | 可用NaOH溶液除去冬青油中少量的水杨酸 |
