题目内容
12.下列对实验操作和实验事实的描述中不正确的说法共有( )①存放浓硝酸时,使用带玻璃塞的棕色玻璃瓶
②不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上稀硼酸溶液
③用托盘天平称量时,所称药品均可放在纸上,并置于天平的左盘
④金属钠着火时,用干沙覆盖灭火
⑤将饱和FeCl3溶液滴入煮沸的稀氢氧化钠溶液中制取氢氧化铁胶体.
| A. | 2个 | B. | 3个 | C. | 4个 | D. | 5个 |
分析 ①浓硝酸光照易分解;
②浓碱溶液沾到皮肤上,要立即用大量水冲洗,降低其浓度;
③称量时,固体在左盘,若为NaOH等放在小烧杯中称量;
④钠与干沙不反应,可隔绝空气灭火;
⑤FeCl3溶液滴入煮沸的稀氢氧化钠溶液中,发生复分解反应生成沉淀.
解答 解:①浓硝酸光照易分解,则存放浓硝酸时,使用带玻璃塞的棕色玻璃瓶,故正确;
②浓碱溶液沾到皮肤上,要立即用大量水冲洗,降低其浓度,然后涂上稀硼酸溶液,操作合理,故正确;
③称量时,固体在左盘,若为NaOH等放在小烧杯中称量,不能所称药品均可放在纸上,故错误;
④钠与干沙不反应,可隔绝空气灭火,操作合理,故正确;
⑤FeCl3溶液滴入煮沸的稀氢氧化钠溶液中,发生复分解反应生成沉淀,则不能制备胶体,应将氯化铁溶液滴到沸水中制备,故错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握试剂的保存、实验安全、基本操作、胶体制备、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
2.下列有关物质的性质与应用相对应的是( )
| A. | 二氧化锰具有强氧化性,可用作H2O2分解的氧化剂 | |
| B. | K2FeO4具有还原性,可用于自来水的杀菌消毒 | |
| C. | Fe3+具有氧化性,可溶解印刷线路板上的金属铜 | |
| D. | SO2具有漂白性,能使紫色KMnO4溶液褪色 |
7.下列各组物质中,所含分子数相同的是( )
| A. | 10g H2和10g O2 | B. | 11.2L(标准状况)H2O和0.5mol Br2 | ||
| C. | 5.6L N2(标准状况)和11g CO2 | D. | 224mL H2(标准状况)和0.1mol N2 |
17.镁、铝、铜三种金属粉末混合物,加入过量盐酸充分反应,过滤后向滤液中加入过量烧碱溶液,再过滤,滤渣中含有( )
| A. | Al(OH)3 | B. | Cu(OH)2 | C. | Mg(OH)2 | D. | Al2O3 |
4.向含有下列4种离子的溶液中加入烧碱固体(溶液体积变化可忽略),能引起离子浓度减小的是( )
| A. | NO3- | B. | Ba2+ | C. | OH- | D. | Cu2+ |
1.将铁粉和铜粉的混合物投入一定量的稀盐酸中,铁粉和铜粉仍有剩余,向反应后的溶液中缓缓地通入氯气.反应分成以下几个阶段:
回答以下问题:
(1)写出第一阶段可能发生的离子反应方程式Fe+2H+=Fe2++H2↑.
(2)第三阶段金属粉末是否有残留可能有.选填(“一定有”、“一定没有”、“可能有”)
(3)第三阶段发生的离子反应方程式是2Fe2++Cl2=2Cl-+Fe3+,2Fe3++Cu=Cu2++2Fe2+(和以上(1)中重复的不写).
(4)第四阶段金属粉末是否有残留?一定没有.选填(“一定有”、“一定没有”、“可能有”)
(5)第五阶段溶液中存在的金属阳离子是Fe3+、Fe2+、Cu2+(写出离子符号).
| 反应阶段 | 溶液中的存在的金属离子 | 残留的金属粉末 | 发生的离子反应 |
| 第一阶段 | 只有一种 | 有两种 | (1) |
| 第二阶段 | 只有一种 | 只有一种 | |
| 第三阶段 | 只有两种 | (2) | (3) |
| 笫四阶段 | 有三种 | (4) | |
| 笫五阶段 | (5) |
(1)写出第一阶段可能发生的离子反应方程式Fe+2H+=Fe2++H2↑.
(2)第三阶段金属粉末是否有残留可能有.选填(“一定有”、“一定没有”、“可能有”)
(3)第三阶段发生的离子反应方程式是2Fe2++Cl2=2Cl-+Fe3+,2Fe3++Cu=Cu2++2Fe2+(和以上(1)中重复的不写).
(4)第四阶段金属粉末是否有残留?一定没有.选填(“一定有”、“一定没有”、“可能有”)
(5)第五阶段溶液中存在的金属阳离子是Fe3+、Fe2+、Cu2+(写出离子符号).
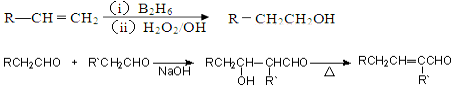
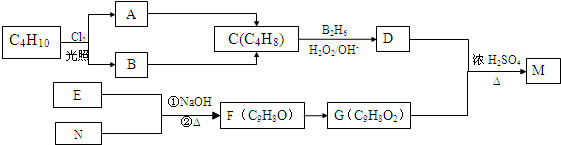
 、
、 ;
; $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$