题目内容
在氧化还原反应KClO3+6HCl═KCl+3Cl2↑+3H2O中,下列说法错误的是( )
| A、KClO3在反应中得到电子 |
| B、HCl是还原剂 |
| C、氧化剂与还原剂的物质的量之比是1:6 |
| D、当生成3mol Cl2时有5mol电子转移 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:KClO3+6HCl═KCl+3Cl2↑+3H2O中,Cl元素的化合价由+5价降低为0,Cl元素的化合价由-1价升高为0,以此来解答.
解答:
解:A.KClO3在反应中,Cl元素的化合价降低,则Cl得到电子,故A正确;
B.HCl中Cl元素的化合价升高,则为还原剂,故B正确;
C.由反应可知,1mol氧化剂与5molHCl转移电子守恒,则氧化剂与还原剂的物质的量之比是1:5,故C错误;
D.当生成3mol Cl2时,1mol氧化剂参加反应,有1mol×(5-0)=5mol电子转移,故D正确;
故选C.
B.HCl中Cl元素的化合价升高,则为还原剂,故B正确;
C.由反应可知,1mol氧化剂与5molHCl转移电子守恒,则氧化剂与还原剂的物质的量之比是1:5,故C错误;
D.当生成3mol Cl2时,1mol氧化剂参加反应,有1mol×(5-0)=5mol电子转移,故D正确;
故选C.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化及发生的反应为解答的关键,侧重氧化还原反应基本概念的考查,注重基础知识的夯实,题目难度不大.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
一包混有杂质的Na2CO3,其杂质只可能是Ba(NO3)2、KCl、NaHCO3、K2CO3中的一种或几种,今取10.6g样品,溶于水得澄清溶液,另取10.6克样品,加入足量的盐酸,收集到4.4gCO2,则下列判断正确的是( )
| A、样品中只混有NaHCO3 |
| B、样品中一定混有NaHCO3,可能混有KCl,也可能混有K2CO3 |
| C、样品中混有NaHCO3,也混有Ba(NO3)2 |
| D、样品中混有KCl,也可能混有NaHCO3 |
下列物质属于电解质的是( )
| A、Cu |
| B、液态NH3 |
| C、CO2 |
| D、Na2O2固体 |
在容积不变的密闭容器中存在如下反应:2SO2(g)+O2(g)?2SO3(g)△H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
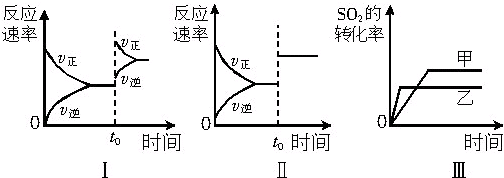

| A、图Ⅰ研究的是t0时刻增大O2的浓度对反应速率的影响 |
| B、图Ⅱ研究的是t0时刻加入催化剂后对反应速率的影响 |
| C、图Ⅲ研究的是催化剂对平衡的影响,且甲的催化效率比乙高 |
| D、图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高 |
下列物质属于糖类且属于高分子化合物的是( )
| A、蔗糖 | B、牛油 |
| C、纤维素 | D、蛋白质 |
有关物质分离、鉴别、制备、除杂的操作正确的是( )
| A、欲分离硝酸钾和氯化钠的混合物(物质的量比为1:1),先将样品溶解,然后加热至表面出现晶膜后再冷却,过滤得硝酸钾晶体;再将母液加热至大量晶体析出后,用余热蒸干,得氯化钠晶体 |
| B、摘下几根火柴头,浸于水中,片刻后取少量溶液于试管中,加AgNO3溶液、稀硝酸,若出现白色沉淀,就说明含有氯元素 |
| C、实验室制取肥皂:将适量植物油、乙醇和NaOH溶液混合,并不断搅拌、加热,直到混合物变稠,即可得到肥皂 |
| D、乙酸乙酯制备实验中,在粗产品中加入饱和Na2CO3溶液处理除去乙酸、乙醇等杂质 |
乙醇汽油(汽油中加入一定比例的乙醇)的使用可以缓解石油危机.从甜菜或甘蔗中提取的蔗糖可以通过发酵产生乙醇.下列过程中没有发生化学变化的是( )
| A、汽油中加入乙醇 |
| B、乙醇的燃烧 |
| C、蔗糖的发酵 |
| D、甜菜的生长 |
某同学写出的下列烃分子的名称,错误的是( )
| A、2,3,4-三甲基己烷 |
| B、2,3-二甲基丁烷 |
| C、2-乙基戊烷 |
| D、3,4-二甲基己烷 |
某烷烃一个分子里含有9个碳原子,其一氯代物只有两种,这种烷烃的名称是( )
| A、正壬烷 |
| B、2,6-二甲基庚烷 |
| C、2,2,4,4-四甲基戊烷 |
| D、2,3,4-三甲基己烷 |