题目内容
4.一定量的甲烷燃烧后得到的产物为二氧化碳、一氧化碳和水蒸气,将产生的气体按顺序通过装有无水氯化钙和氢氧化钠的硬质玻璃管,氢氧化钠管的质量增加了4.4g,则甲烷在标准状况下的体积是多少,无水氯化钙的质量增加了 ( )| A. | 0.56L 1.8g | B. | 1.12L 3.6g | C. | 2.24L 1.8g | D. | 2.24L 3.6g |
分析 甲烷燃烧生成二氧化碳与水,无水CaCl2吸收生成的水,NaOH吸收生成的二氧化碳,根据n=$\frac{m}{M}$计算二氧化碳的物质的量,根据碳原子守恒计算甲烷物质的量,再根据V=nVm计算甲烷体积;无水氯化钙的质量增加的质量即为生产水的质量.
解答 解:甲烷燃烧生成二氧化碳与水,无水CaCl2吸收生成的水,NaOH吸收生成的二氧化碳,即生成二氧化碳的质量为4.4g,二氧化碳的物质的量=$\frac{4.4g}{44g/mol}$=0.1mol,根据碳原子守恒,甲烷物质的量=0.1mol,故标况下,甲烷体积=0.1mol×22.4L/mol=2.24L,根据氢原子守恒则n(H2O)=2n(CH4)=0.2mol,m(H2O)=0.2×18=3.6g,故无水氯化钙的质量增加了3.6g,故选D.
点评 本题考查化学方程式有关计算,比较基础,判断二氧化碳质量是关键,注意利用原子守恒计算,简化计算步骤.

练习册系列答案
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
10.某小组为研究电化学原理,设计如图装置.下列叙述正确的是( )
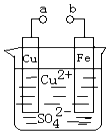

| A. | a和b不连接时,铁片上会有金属铜析出 | |
| B. | a和b用导线连接时,铁片上发生的反应为:Fe-3e-═Fe3+ | |
| C. | 无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 | |
| D. | a和b用导线连接后,铁片上发生还原反应,溶液中铜离子向铜电极移动 |
8.核内中子数为N的R2+,质量数为A,则n g它的氧化物中所含质子的物质的量是( )
| A. | $\frac{n}{A+16}$(A-N+8)mol | B. | $\frac{n}{A+16}$(A-N+10)mol | C. | $\frac{n}{A}$ (A-N+2)mol | D. | $\frac{n}{A}$(A-N+6)mol |
15.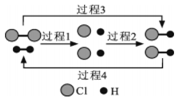 H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列属于吸热过程的是 ( )
H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列属于吸热过程的是 ( )
 H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列属于吸热过程的是 ( )
H2 能在Cl2中燃烧生成 HCl,HCl也能在一定条件下分解为H2和Cl2. 图为H2、Cl2和HCl 三者相互转化的微观过程示意图,下列属于吸热过程的是 ( )| A. | 过程 1 | B. | 过程 2 | C. | 过程 3 | D. | 过程 4 |
9.下列分离或提纯物质的方法、操作正确的是( )
| A. | 用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 用过滤的方法除去NaCl溶液中含有的少量淀粉胶体 | |
| D. | 将制得晶体转移到新制过滤器中用大量水进行洗涤 |
13.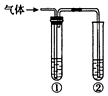 用下图装置完成下列实验,不需要试管①(内盛有相应的除杂试剂)就能达到实验目的是( )
用下图装置完成下列实验,不需要试管①(内盛有相应的除杂试剂)就能达到实验目的是( )
 用下图装置完成下列实验,不需要试管①(内盛有相应的除杂试剂)就能达到实验目的是( )
用下图装置完成下列实验,不需要试管①(内盛有相应的除杂试剂)就能达到实验目的是( ) | 实验目的 | ②中的试剂 | |
| A | 检验碳与浓硫酸反应产生的气体中含有二氧化碳 | 澄清石灰水 |
| B | 用碳酸钙与盐酸反应产生的气体验证碳酸的酸性强于苯酚 | 苯酚钠溶液 |
| C | 验证乙醇在浓硫酸作用下发生消去反应产生的气体为不饱和烃 | 酸性高锰酸钾溶液 |
| D | 验证石蜡油在碎瓷片上受热分解产生的气体中含有不饱和烃 | 溴的四氯化碳溶液 |
| A. | A | B. | B | C. | C | D. | D |
14.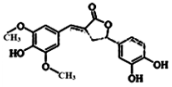 天然有机化合物甲的结构简式如图,该物质具有一定的除草功效,有关该化合物的说法正确的是( )
天然有机化合物甲的结构简式如图,该物质具有一定的除草功效,有关该化合物的说法正确的是( )
 天然有机化合物甲的结构简式如图,该物质具有一定的除草功效,有关该化合物的说法正确的是( )
天然有机化合物甲的结构简式如图,该物质具有一定的除草功效,有关该化合物的说法正确的是( )| A. | 既能与FeCl3发生显色反应,也能和NaHCO3反应放出CO2 | |
| B. | 1 mol该化合物最多能与6 mol NaOH 反应 | |
| C. | 1 mol 该化合物最多能与含5 mol Br2的浓溴水反应 | |
| D. | 该化合物分子中含有三种含氧官能团 |
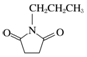 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂任选).合成路线流程图示例如下: