题目内容
下列离子方程式中正确的是( )
| A、用氯化铁溶液腐蚀铜板:Fe3++Cu=Fe2++Cu2+ |
| B、将少量的二氧化硫气体通入次氯酸钠溶液中 SO2+H2O+2ClO-=SO32-+2HClO |
| C、用氢氧化钡溶液中和硫酸氢铵溶液:H++SO42-+Ba2++OH-=H2O+BaSO4↓ |
| D、用纯碱溶液溶解苯酚:CO32-+C6H5OH→HCO3-+C6H5O- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.电荷不守恒;
B.次氯酸具有强氧化性,将二氧化硫氧化成硫酸根;
C.离子个数不符合物质的配比;
D.碳酸钠与苯酚反应生成碳酸氢钠和苯酚钠.
B.次氯酸具有强氧化性,将二氧化硫氧化成硫酸根;
C.离子个数不符合物质的配比;
D.碳酸钠与苯酚反应生成碳酸氢钠和苯酚钠.
解答:
解:A.用氯化铁溶液腐蚀铜板,离子方程式:2Fe3++Cu=2Fe2++Cu2+,故A错误;
B.将少量二氧化硫气体通入次氯酸钠溶液中,离子方程式:SO2+ClO-+H2O=SO42-+2H++Cl-,故B错误;
C.用氢氧化钡溶液中和硫酸氢铵溶液,离子方程式:2H++SO42-+Ba2++2OH-=2H2O+BaSO4↓,故C错误;
D.碳酸钠与苯酚反应生成碳酸氢钠和苯酚钠,离子方程式:CO32-+C6H5OH→HCO3-+C6H5O-,故D正确;
故选:D.
B.将少量二氧化硫气体通入次氯酸钠溶液中,离子方程式:SO2+ClO-+H2O=SO42-+2H++Cl-,故B错误;
C.用氢氧化钡溶液中和硫酸氢铵溶液,离子方程式:2H++SO42-+Ba2++2OH-=2H2O+BaSO4↓,故C错误;
D.碳酸钠与苯酚反应生成碳酸氢钠和苯酚钠,离子方程式:CO32-+C6H5OH→HCO3-+C6H5O-,故D正确;
故选:D.
点评:本题考查了离子方程式的正误判断和注意问题,明确物质的性质及离子方程式书写规则即可解答,选项B为易错选项.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案
相关题目
下列关于醇与酚的比较中正确的是( )
| A、醇和酚都能与氢氧化钠溶液反应 |
| B、醇和酚都能与钠发生反应 |
| C、醇、酚的水溶液都能使石蕊试纸变红 |
| D、醇和酚都能与碳酸钠溶液反应 |
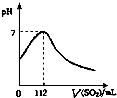 在标准状况下,向100mL氢硫酸溶液中通入二氧化硫气体,溶液pH变化如图所示,则原氢硫酸溶液的物质的量浓度为( )
在标准状况下,向100mL氢硫酸溶液中通入二氧化硫气体,溶液pH变化如图所示,则原氢硫酸溶液的物质的量浓度为( )| A、0.5 mol?L─1 |
| B、0.05 mol?L─1 |
| C、1 mol?L─1 |
| D、0.1 mol?L─1 |
设NA 代表阿伏加德罗常数(NA)的数值,下列说法正确的是( )
| A、1 mol 硫酸钾中阴离子所带电荷数为NA |
| B、乙烯和环丙烷(C3H6)组成的28g混合气体中含有NA个氢原子 |
| C、标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为NA |
| D、将0.1mol氯化铁溶于1L水中,所得溶液含有0.1NA Fe3+ |
下列离子方程式中正确的是( )
| A、氯化铝溶液中加入过量氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| B、AlCl3 溶液中投入过量Na:Al3++4Na+2H2O=AlO2-+4Na++2H2↑ |
| C、苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
| D、碳酸氢铵溶液中加入过量氢氧化钠溶液:HCO3-+OH-=CO32-+H2O |
某物质在酸性条件下可以发生水解反应生成两种物质A、B,且A和B的相对分子质量相等,该物质可能是( )
| A、甲酸乙酯(HCOOC2H5) |
| B、乙酸乙酯(CH3COOC2H5) |
| C、葡萄糖(C6H12O6) |
| D、淀粉〔(C6H10O5)n〕 |