题目内容
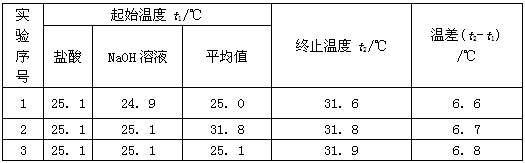
某实验上组设计用50 mL 0.5 mol/L盐酸跟50 mL 0.55 mol/L氢氧化钠溶液在下图装置中进行中和反应.通过测定反应过程中所放出的热量来计算中和热.试回答下列问题:

(1)实验装置图中的错误有:
①________②________③________(可不填满,也可补充)
(2)烧杯间填满碎泡沫塑料或碎纸条的作用是________________
(3)本实验中用稍过量的NaOH的原因,教材中说是为保证盐酸完全被中和.试问:盐酸在反应中若因为有放热现象,而造成少量盐酸在反应中挥发,则测得的中和热数值将________(填“偏高”、“偏低”或“不变”)
(4)实验中如改用50 ml 0.6 mol/L盐酸跟50 ml 0.55 mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量________,所求得的中和热数值________.(以上两空填“相等”或“不相等”).
答案:
解析:
解析:
(1)①缺少环形玻璃棒 ②小烧杯口未与大烧杯口平齐
(2)保温隔热,减少实验过程中热量损失
(3)偏低
(4)不相等,相等

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目

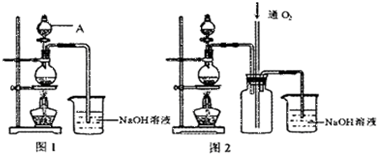

 Si(s)+4HCl(g)?该反应的反应热ΔH=
Si(s)+4HCl(g)?该反应的反应热ΔH=