题目内容
25℃时,三种难溶银盐的Ksp与颜色如表,下列说法正确的是( )
| AgCl | Ag2CrO4 | AgI | |
| 颜色 | 白 | 砖红 | 黄 |
| Ksp | 1.8×10-10 | 1.0×10-12 | 8.5×10-17 |
| A、AgCl、Ag2CrO4、AgI饱和溶液中c(Ag+)依次减弱 |
| B、Ag2CrO4饱和溶液中c(Ag+)约为1.0×10-6mol?L-1 |
| C、向AgCl悬浊液加入足量KI溶液,沉淀将由白色转化为黄色 |
| D、向等浓度的KCl与K2CrO4混合溶液中滴加少量AgNO3溶液,将生成砖红色沉淀 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:A.由表中数据可知溶度积AgCl饱和溶液中c(Ag+)=
=
×10-5mol/L,其溶解度也最大,Ag2CrO4饱和溶液中:c(Ag+)=
=
×10-4mol/L;
B.Ag2CrO4饱和溶液中:c(Ag+)=
=
×10-4mol/L;
C.AgI溶度积小于AgCl,溶解度小的沉淀转化为溶解度更小的容易实现,所以向AgCl悬浊液加入足量KI溶液,可能有黄色沉淀产生;
D.由A可知,饱和溶液中c(Ag+):AgCl<Ag2CrO4,向等浓度的KCl与K2CrO4混合溶液中滴加少量AgNO3溶液,将生成白色沉淀.
| 1.8×10-10 |
| 1.8 |
| 3 | 2×1×10-12 |
| 3 | 2 |
B.Ag2CrO4饱和溶液中:c(Ag+)=
| 3 | 2×1×10-12 |
| 3 | 2 |
C.AgI溶度积小于AgCl,溶解度小的沉淀转化为溶解度更小的容易实现,所以向AgCl悬浊液加入足量KI溶液,可能有黄色沉淀产生;
D.由A可知,饱和溶液中c(Ag+):AgCl<Ag2CrO4,向等浓度的KCl与K2CrO4混合溶液中滴加少量AgNO3溶液,将生成白色沉淀.
解答:
解:A.由表中数据可知溶度积AgCl饱和溶液中c(Ag+)=
=
×10-5mol/L,其溶解度也最大,Ag2CrO4饱和溶液中:c(Ag+)=
=
×10-4mol/L,故A错误;
B.Ag2CrO4饱和溶液中:c(Ag+)=
=
×10-4mol/L,故B错误;
C.AgI溶度积小于AgCl,溶解度小的沉淀转化为溶解度更小的容易实现,所以向AgCl悬浊液加入足量KI溶液,可能有黄色沉淀产生,故C正确;
D.由A可知,饱和溶液中c(Ag+):AgCl<Ag2CrO4,向等浓度的KCl与K2CrO4混合溶液中滴加少量AgNO3溶液,将生成白色沉淀,故D错误;
故选C.
| 1.8×10-10 |
| 1.8 |
| 3 | 2×1×10-12 |
| 3 | 2 |
B.Ag2CrO4饱和溶液中:c(Ag+)=
| 3 | 2×1×10-12 |
| 3 | 2 |
C.AgI溶度积小于AgCl,溶解度小的沉淀转化为溶解度更小的容易实现,所以向AgCl悬浊液加入足量KI溶液,可能有黄色沉淀产生,故C正确;
D.由A可知,饱和溶液中c(Ag+):AgCl<Ag2CrO4,向等浓度的KCl与K2CrO4混合溶液中滴加少量AgNO3溶液,将生成白色沉淀,故D错误;
故选C.
点评:本题考查难溶电解质的溶解平衡问题,题目难度不大,本题注意比较表中数据,把握溶解平衡的特征以及影响因素.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
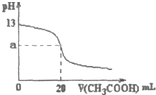 向20.OOmLO.lmol?L-1的NaOH溶液中逐滴加入0.lOOmol.L-1 CH3COOH溶液,滴定曲线如图,下列有关叙述正确的是( )
向20.OOmLO.lmol?L-1的NaOH溶液中逐滴加入0.lOOmol.L-1 CH3COOH溶液,滴定曲线如图,下列有关叙述正确的是( )| A、0.lOOmol?L-1的CH3COOH溶液的pH=l |
| B、如图a=7 |
| C、当V<20.00mL时,溶液中离子浓度的大小关系可能为:c(CH3CO0-)>c(Na+)>(OH-)>c(H+) |
| D、当V=20.00mL时.有c(CH3COO-)+c(CH3COOH)=c(Na+) |
下列叙述不正确的是( )
| A、铜具有良好的导电性,常用来制作印刷电路板 |
| B、硅和二氧化硅都是重要的半导体材料 |
| C、铝制品不宜长时间盛放酸性或碱性食物 |
| D、氯水和过氧化钠都具有漂白作用,其漂白原理相同 |
下列物质中,能跟NaOH溶液反应放氢气的是( )
| A、Mg | B、Al |
| C、S | D、Cl2 |
下列各物质分别滴加浓硫酸后,现象描述正确的是( )
| A、胆矾晶体由蓝色变无色 |
| B、pH试纸变红 |
| C、蓝色石蕊试液褪色 |
| D、白纸变黑 |
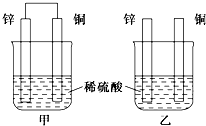 将纯锌片和纯铜片按下图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
将纯锌片和纯铜片按下图方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题: