题目内容
3.下列实验中,利用了盐酸的氧化性的是( )| A. | 用盐酸除去铜粉中混有的铁粉 | |
| B. | 用浓盐酸和MnO2制氯气 | |
| C. | 用盐酸跟氢氧化钠溶液反应 | |
| D. | 盐酸和硝酸银溶液反应生成白色沉淀 |
分析 HCl中H元素的化合价为+1价,当发生化学反应时,H元素的化合价降低,H元素被还原时,则盐酸表现出氧化性,据此进行解答.
解答 解:A.用盐酸除去铜粉中混有的铁粉,发生反应为:2HCl+Fe=FeCl2+H2↑,H元素的化合价由+1价降低为0价,则盐酸表现为氧化性,故A正确;
B.用浓盐酸和MnO2制氯气,盐酸中氯离子被氧化成氯气,盐酸作还原剂,故B错误;
C.盐酸跟氢氧化钠溶液反应,为酸碱的中和反应,各元素的化合价都没有变化,盐酸表现为酸性,故C错误;
D.盐酸和硝酸银溶液反应生成白色沉淀,发生复分解反应,各元素的化合价都没有变化,故D错误;
故选A.
点评 本题考查氧化还原反应,题目难度不大,注意从化合价变化的角度判断反应中盐酸的作用,明确氧化剂、还原剂的概念及发生变化为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
相关题目
14.将8.7gMnO2与足量的浓盐酸共热来制取氯气.有关说法正确的为( )
| A. | 可制得14.2g氯气 | B. | 被氧化的HCl的质量为14.6g | ||
| C. | 被氧化的HCl的质量为7.3g | D. | 转移的电子的物质的量为0.2mol |
8.下列物质的保存方法不正确的是( )
| A. | 少量金属钠保存在煤油中 | |
| B. | 浓硝酸盛放在无色瓶中 | |
| C. | 少量白磷保存在冷水中 | |
| D. | 氢氧化钠溶液盛放在橡胶塞的试剂瓶中 |
15.下列说法正确的是( )
| A. | 碳原子间以单键相连的链烃是烷烃 | B. | 所有糖类物质都有甜味 | ||
| C. | 糖类、油脂都能发生水解 | D. | 淀粉与纤维素互为同分异构体 |
13.下列说法正确的是( )
| A. | 用PH试纸测得某浓度的Na2CO3溶液的PH值为10.2 | |
| B. | 已知Na2S2O3+H2SO4═Na2SO4+S↓+SO2↑+H2O,在定量测定该反应速率时,可用排水法测SO2的体积,计算反应速率 | |
| C. | 蒸发结晶时,将蒸发皿中的溶液蒸干后得到所需固体 | |
| D. | 脂皂化反应后的反应液中加入饱和食盐水并搅拌后,生成的高级脂肪酸钠浮在水面 |
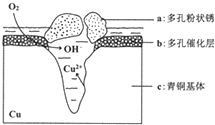 我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器因受到环境腐蚀,欲对其进行修复和防护具有重要意义.
我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器因受到环境腐蚀,欲对其进行修复和防护具有重要意义.