题目内容
用Na2CO3沉淀CaCl2溶液中的钙离子,如何检验Ca2+已经沉淀完全 .
考点:物质的检验和鉴别的实验方案设计
专题:物质检验鉴别题
分析:Ca2+已经沉淀完全,则Na2CO3过量,溶液中含有碳酸根离子,可以根据碳酸根离子的特征离子反应:可用盐酸或钙离子反应生成碳酸钙沉淀来检验碳酸根离子.
解答:
解:CaCl2和Na2CO3反应生成碳酸钙和氯化钠,Na2CO3已过量则氯化钙无剩余,可以取向反应后的上层溶液少许,再加入Na2CO3溶液,若不产生白色沉淀,则可确认Na2CO3已过量,或取上清液加入盐酸,如产生气泡,说明碳酸根离子过量,Ca2+已经沉淀完全,也可加入氯化钙,如生成沉淀,也可说明碳酸根离子过量,Ca2+已经沉淀完全,
故答案为:沉淀反应后,用试管取出上层清液,再加入Na2CO3溶液,若产生白色沉淀,则可确认Na2CO3已过量.
故答案为:沉淀反应后,用试管取出上层清液,再加入Na2CO3溶液,若产生白色沉淀,则可确认Na2CO3已过量.
点评:本题考查物质的检验,侧重于学生的分析能力的考查,为高频考点,难度不大,注意把握物质的性质以及实验操作方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
铁铬氧化还原液流电池是一种低成本的储能电池,电池结构如图所示,工作原理为Fe3++Cr2+
Fe2++Cr3+.下列说法一定正确的是( )
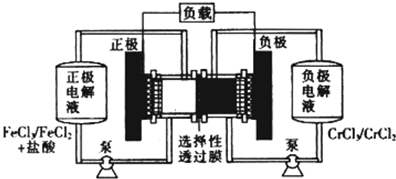
| 放电 |
| 充电 |

| A、充电时,阴极的电极反应式为Cr3++e-=Cr2+ |
| B、电池放电肘,负极的电极反应式为Fe2+-e-=Fe3+ |
| C、电池放电时,Cl-从负极室穿过选择性透过膜移向正极室 |
| D、放电时,电路中每流过0.1 mol电子,Fe3+浓度降低0.1mol.L-1 |
化学用语是学习化学的重要工具.以下化学用语或表述正确的是( )
| A、乙烯的结构简式:CH2CH2 |
B、碳正离 中质子数与电子数之比值为3:2 中质子数与电子数之比值为3:2 |
| C、钙离子的基态电子排布比:1s22s22p63s23p6 |
| D、NaHCO3水解反应的离子方程式:HCO3-+H2O?H3O++CO32- |
下列离子方程式书写正确的是( )
| A、将铜屑加入FeCl3溶液中:Fe3++Cu=Fe2++Cu2+; |
| B、向明矾溶液中加入少量氢氧化钡溶液:Al3++SO42-+Ba2++3OH-=BaSO4↓+Al(OH)3↓ |
| C、向硫酸铜加入过量氨水中:Cu2++4NH3=[Cu(NH3)4]2+ |
| D、少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO |


 已知,中学化学常见的一些物质有如下图转化关系(转化关系中的某些产物已略去).其中,物质A、D、G是单质,D的单质在黄绿色气体中燃烧生成的产物溶于水得到E,黑色物质C有磁性是某金属矿物的主要成份,F是混合物,H是极易溶于水的碱性气体.
已知,中学化学常见的一些物质有如下图转化关系(转化关系中的某些产物已略去).其中,物质A、D、G是单质,D的单质在黄绿色气体中燃烧生成的产物溶于水得到E,黑色物质C有磁性是某金属矿物的主要成份,F是混合物,H是极易溶于水的碱性气体.