题目内容
9.实验室里通常用MnO2与浓盐酸反应制取氯气,现要制取标准状况下11.2L氯气,请完成:(1)写出实验室制取氯气的化学方程式:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)理论上需要MnO2固体的质量是多少?(浓盐酸过量)
(3)被还原的HCl的物质的量是多少?
分析 实验室用二氧化锰与浓盐酸在加热条件下制备氯气,反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,计算生成氯气的物质的量,根据方程式计算需要二氧化锰的物质的量,再根据m=nM计算二氧化锰的质量,被氧化的HCl生成氯气,根据氯原子守恒计算被氧化HCl的物质的量.
解答 解:(1)实验室用二氧化锰与浓盐酸在加热条件下制备氯气,反应方程式为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)11.2L 氯气的物质的量为$\frac{11.2L}{22.4L/mol}$=0.5mol,
MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O
1 1
0.5mol 0.5mol
故需要二氧化锰的质量为0.5mol×87g/mol=43.5g,
答:理论上需要MnO2固体的质量是43.5g;
(3)被氧化的HCl生成氯气,根据氯原子守恒,被氧化HCl的物质的量为0.5mol×2=1mol,
答:被氧化的HCl的物质的量为1mol.
点评 本题考查氧化还原反应计算、化学方程式的计算,比较基础,注意根据化合价理解氧化还原反应基本概念,注意根据电子转移守恒进行氧化还原反应的有关计算.

练习册系列答案
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
13.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 28g乙烯或丙烯完全燃烧均生成2NACO2 | |
| B. | 在标准状况下,11.2L氖气含有的氖原子数为NA | |
| C. | 78gNa2O2跟水充分反应,转移的电子数为2NA | |
| D. | 1L 1mol/L CH3COONa溶液中存在NA个CH3COO |
20.如图所示的装置能够组成原电池的是( )
| A. | 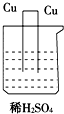 | B. | 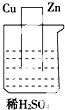 | C. | 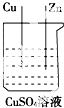 | D. | 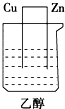 |
17.“春蚕到死丝方尽,蜡炬成灰泪始干.”中的“丝”和“泪”分别是指( )
| A. | 油脂,纤维素 | B. | 蛋白质,烃 | C. | 纤维素,烃 | D. | 蛋白质,油脂 |
14.下列A、B两种元素的原子序数,其中可以组成AB2型离子化合物的( )
| A. | 6和8 | B. | 19和16 | C. | 12和17 | D. | 7和8 |
1.常温下,现有电解质溶液:①NaClO ②NaOH ③NaHCO3 ④CH3COONa,当几种溶液的pH相同时,其物质的量浓度由大到小的顺序排列正确的是( )
| A. | ②①③④ | B. | ①③④② | C. | ④③①② | D. | ③④②① |
19.下列离子组一定能够大量共存的是( )
| A. | 含ClO-的溶液中:Fe3+、S042-、NO3-、K+ | |
| B. | 使石蕊试液显红色的溶液中:Fe2+、K+、NO3-、CI- | |
| C. | 在c(H+):c(OH-)=1:1012的溶液中,Na+、I-、NO3-、SO42- | |
| D. | 能使有色布条褪色的溶液:K+、S032-、NO3-、Mg2+ |
 .
.