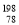题目内容
用NA表示阿伏加德罗常数,下列说法中正确的是( )
①46g NO2和N2O4的混合气体中含有的原子个数为3NA
②常温下,4 g CH4含有NA个C-H共价键
③10 mL质量分数为98%的H2SO4,加水至100 mL,H2SO4的质量分数为9.8%
④标准状况下,5.6L四氯化碳含有的分子数为0.25NA
⑤25 ℃时,pH=12的1.0 L NaClO溶液中水电离出的OH-的数目为0.01NA
⑥0.lmol·L-1Na2CO3溶液中含有0.1NA个CO32-
⑦1 mol Na2O2与水完全反应时转移电子数为2NA
A.③⑥⑦ B.①②⑤ C.①②④ D.④⑤⑥
B
【解析】
试题分析:①NO2和N2O4的最简式相同,均是NO2,所以46g NO2和N2O4的混合气体中相对于含有1molNO2,则其中含有的原子个数为3NA,正确;②常温下,4 g CH4的物质的量是0.25mol,含有NA个C-H共价键,正确;③硫酸的密度随浓度的增大而增大,所以10 mL质量分数为98%的H2SO4,加水至100 mL,H2SO4的质量分数大于9.8%,错误;④标准状况下四氯化碳是液态,不能适用于气体摩尔体积,则5.6L四氯化碳含有的分子数不是0.25NA,错误;⑤25 ℃时,pH=12的1.0 L NaClO溶液中氢氧根的浓度是0.01mol/L,则水电离出的OH-的数目为0.01NA,正确;⑥不能确定碳酸钠溶液的体积,因此不能计算0.lmol·L-1Na2CO3溶液中碳酸钠的物质的量,错误;⑦1 mol Na2O2与水完全反应时转移电子数为NA,错误,答案选B。
考点:考查阿伏伽德罗常数的计算

 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案( I) 在一个容积固定不变的密闭容器中进行反应:
2X(g) + Y(g)  2Z(g) 若把2molX和1molY充入该容器时,处于状 态I, 反应在绝热条件下达到平衡时处于状态II(如下图),则该反应的△H 0; ( 填:“< ,> , = ”)。该反应在 (填:高温或低温)条件下能自发进行。
2Z(g) 若把2molX和1molY充入该容器时,处于状 态I, 反应在绝热条件下达到平衡时处于状态II(如下图),则该反应的△H 0; ( 填:“< ,> , = ”)。该反应在 (填:高温或低温)条件下能自发进行。
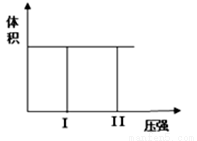
(II)在容积可变的密闭容器中发生反应:mA(g) + nB(g)  pC(g) ,
pC(g) ,
在一定温度和不同压强下达到平衡时,分别得到A的物质的量浓度如
下表
压强p/Pa | 2×105 | 5×105 | 1×106 |
c(A)/mol·L-1 | 0.08 | 0.20 | 0.44 |
(1)当压强从2×105 Pa增加到5×105 Pa时,平衡 移动(填:向左, 向右 ,不)
(2)维持压强为2×105 Pa,当反应达到平衡状态时,体系中共有amol气体,再向体系中加入bmolB,当重新达到平衡时,体系中气体总物质的量是 mol.
(3)当压强为1×106 Pa时,此反应的平衡常数表达式: 。
(4)其他条件相同时,在上述三个压强下分别发生该反应。2×105 Pa时,
A的转化率随时间变化如下图,请在图中补充画出压强分别为5×105 Pa
和1×106 Pa时,A的转化率随时间的变化曲线(请在图线上标出压强)。

下列事实不能用平衡移动原理解释的是( )
2SO2+O2 的平衡体系中,加入由18O构成的氧气,则SO2中的18O的含量会增加 |
|
|
| ||||||||||||
A | B | C | D |
(10分)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
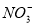 +4H++3e-=NO+2H2O。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
+4H++3e-=NO+2H2O。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:______________。
(2)反应中硝酸体现了________、_________的性质。
(3)反应中若产生0.2 mol气体,则转移电子的物质的量是___________mol。
(4)若1 mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是___________。
下列有关微粒之间关系和特征描述正确的是( )。
选项 | 微粒 | 相互关系 | 特征描述 |
A | C60、C70、C540 | 同位素 | 微粒中只含非极性共价键 |
B | 新戊烷、2,2-二甲基丙烷 | 同分异构体 | 常温常压下呈气态 |
C | 同素异形体 | 铂作氨催化氧化时的催化剂 | |
D | 甲酸、硬脂酸 | 同系物 | 能发生酯化反应 |
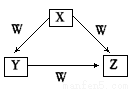
X 、Y、Z、W是中学化学常见的四种物质,他们之间具有如图所示转化关系,则下列组合不可能的是
| X | Y | Z | W |
A | C | CO | CO2 | O2 |
B | Na | Na2O | Na2O2 | O2 |
C | AlCl3 | Al(OH)3 | NaAl(OH)4 | NaOH |
D | Fe | FeCl2 | FeCl3 | Cl2 |
 2SO3
2SO3