题目内容
4.氮及其化合物在生产、生活中具有重要作用.(1)利用NH3的还原性可消除氮氧化物的污染,相关热化学方程式如下:
H2O(l)=H2O(g)△H1=+44.0kJ•mol-1
N2(g)+O2(g)=2NO(g)△H2=+229.3kJ•mol-1
4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H3=-906.5kJ•mol-1
则:4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H4=-2317kJ•mol-1.
(2)使用NaBH4为诱导剂,可使Co2+与肼(N2H4)在碱性条件下发生反应,制得高纯度纳米钴,并产生可参与大气循环的气体
①写出该反应的离子方程式:2Co2++N2H4+4OH-=2Co↓+N2↑+4H2O.
②在纳米钴的催化作用下,肼可分解生成两种气体,其中一种能使湿润的红色石蕊试纸变蓝.若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如图1所示,则肼分解反应的化学平衡常数的表达式为:$\frac{c({N}_{2}){c}^{4}(N{H}_{3})}{{c}^{3}({N}_{2}{H}_{4})}$;为抑制肼的分解,可采取的合理措施有降低反应温度(任写一种).
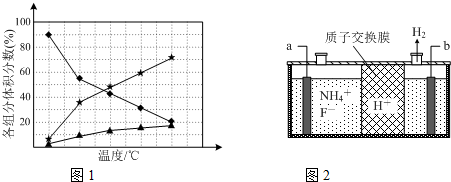
(3)NF3在微电子工业上常用作蚀刻剂,在对硅、氮化硅等材料进行蚀刻时,具有非常优异的蚀刻速率和选择性,且在被蚀刻物表面无物质残留,不会污染表面.工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如图2所示.
①a电极为电解池的阳极,该电极的电极反应式为NH4++3F--6e-=NF3+4H+.
②以NF3蚀刻Si3N4为例,解释被蚀刻物表面无物质残留的原因是4NF3+Si3N4=4N2↑+3SiF4↑.
③NF3能与水发生反应,生成两种酸及一种气态氧化物,其中两种酸分别是HF和HNO3.
分析 (1)H2O(l)=H2O(g)△H1=44.0kJ•mol-1 (i)
N2(g)+O2(g)=2NO(g)△H2=229.3kJ•mol-1 (ii)
4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H3=-906.5kJ•mol-1 (iii)
由盖斯定律可知(iii)-(ii)×5-(i)×6得:4NH3(g)+6NO(g)=5N2(g)+6H2O(l);
(2)①依据题意,反应物为Co2+与肼(N2H4)、碱性条件下存在OH-,生成物为:钴单质,据此得出Co的化合价降低,故N的化合价升高,只能为0价,即氮气,依据氧化还原反应得失电子守恒回答即可;
②使湿润的红色石蕊试纸变蓝的气体为氨气,平衡常数K=$\frac{生成物平衡浓度幂次方乘积}{反应物平衡浓度幂次方乘积}$,由图1得知:温度越高,肼的百分含量越低,即分解的越快;
(3)①电解含NH4F等的无水熔融物生产NF3,N元素被氧化,则a为阳极;
②NF3与Si3N4发生氧化还原反应,生成氮气和四氟化硅,无残留;
③NF3与水反应生成硝酸和HF酸,方程式为3NF3+5H2O=2NO↑+9HF+HNO3.
解答 解:(1)H2O(l)=H2O(g)△H1=44.0kJ•mol-1 (i)
N2(g)+O2(g)=2NO(g)△H2=229.3kJ•mol-1 (ii)
4NH3(g)+5O2(g)=4NO(g)+6H2O(g)△H3=-906.5kJ•mol-1 (iii)
(iii)-(ii)×5-(i)×6得:4NH3(g)+6NO(g)=5N2(g)+6H2O(l),故△H4=-906.5-(229.3×5)-(44×6)=-2317kJ•mol-1,
故答案为:-2317;
(2)①依据题意,反应物为Co2+与肼(N2H4)、碱性条件下存在OH-,生成物为:钴单质,据此得出Co的化合价降低,故N的化合价升高,只能为0价,即氮气,据此得出还有水生成,氧化还原反应中存在得失电子守恒以及元素守恒,故此反应的离子反应方程式为:2Co2++N2H4+4OH-=2Co↓+N2↑+4H2O,
故答案为:2Co2++N2H4+4OH-=2Co↓+N2↑+4H2O;
②使湿润的红色石蕊试纸变蓝的气体为氨气,即肼分解生成氨气,依据元素守恒得知另外一种产物为氮气,故化学反应方程式为:3N2H4$\frac{\underline{催化剂}}{△}$N2+4NH3,平衡常数K=$\frac{生成物平衡浓度幂次方乘积}{反应物平衡浓度幂次方乘积}$=$\frac{c({N}_{2}){c}^{4}(N{H}_{3})}{{c}^{3}({N}_{2}{H}_{4})}$,由图1可知,温度越高,肼的体积分数含量越低,故要抑制肼的分解,应降低反应温度,
故答案为:$\frac{c({N}_{2}){c}^{4}(N{H}_{3})}{{c}^{3}({N}_{2}{H}_{4})}$;降低反应温度;
(3)①电解含NH4F等的无水熔融物生产NF3,N元素被氧化,则a为阳极,发生NH4++3F--6e-=NF3+4H+,
故答案为:阳;NH4++3F--6e-=NF3+4H+;
②NF3与Si3N4发生氧化还原反应,反应方程式为4NF3+Si3N4=4N2↑+3SiF4↑,生成氮气和四氟化硅,无残留,
故答案为:4NF3+Si3N4=4N2↑+3SiF4↑;
③NF3与水反应生成硝酸和HF酸,方程式为3NF3+5H2O=2NO↑+9HF+HNO3,
故答案为:HF和HNO3.
点评 本题考查较为综合,涉及盖斯定律的应用、氧化还原反应方程式书写、电解池反应原理等知识,为高频考点,侧重于学生的分析、计算能力的考查,综合性较强,难度较大,注意相关知识的整理归纳.

 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案| A. | “水玻璃”长期暴露在空气中会变质,这是因为“水玻璃”与空气中的二氧化碳接触,生成 了乳白色的凝胶状沉淀(用H2SiO3表示)和碳酸钠的缘故 | |
| B. | 水的物理性质十分特殊.水的比热容较大,水结成冰后密度变小,水的熔沸点较高等特殊 性质是由于水分子间存在一种被称为氢键的特殊的分子间作用力 | |
| C. | 铅蓄电池是最常见的二次电池,由于它的性能优良、价格低廉、安全可靠,可多次充放电,所以使用广泛,但铅蓄电池也存在比能量低,废弃电池污染环境等缺点 | |
| D. | 硅晶体是一种重要的半导体材料,在常温下,单质硅易与氧气反应,所以自然界中不存在 游离态的硅.石墨烯作为目前发现的最薄、强度最大、导电导热性能最强的一种新型纳米材 料,最有潜力的应用是成为硅的替代品,用来生产未来的超级计算机 |
| A. | 化合物XZ2中,各原子均满足8电子的稳定结构 | |
| B. | 元素X与氢元素能形成原子数目之比为1:1的化合物 | |
| C. | Y的单质与稀硫酸、浓硫酸均可发生氧化还原反应 | |
| D. | Z的单质在加热条件下会与Fe反应生成Fe3Z4 |
| A. | 原子半径:X>W>Z>Y | |
| B. | 化合物ZW3溶于水时水解生成一种弱碱和一种强酸 | |
| C. | X的最高价氧化物能与Z的最高价氧化物对应的水化物反应 | |
| D. | 甲、乙混合时生成的白烟为离子化合物,且该化合物只含有离子键 |
| A. | 标准状况下,78g Na2O2的分子数为NA | |
| B. | 标准状况下,22.4L氯气在任何反应中转移电子数均为2NA | |
| C. | 标准状况下,22.4mL H2O中含水分子的个数约为1.24NA | |
| D. | 17g NH3溶于水后溶质NH3的个数为NA |
| A. | 2:1:2:3 | B. | 2:1:4:6 | C. | 2:1:4:3 | D. | 1:1:1:1 |
| 容器 | 温度/℃ | 物质的起始浓度/mol•L-1 | 物质的平衡浓度/mol•L-1 | ||
| c(H2) | c(CO) | c(CH3OH) | c(CH3OH) | ||
| Ⅰ | 400 | 0.20 | 0.10 | 0 | 0.080 |
| Ⅱ | 400 | 0.40 | 0.20 | 0 | |
| Ⅲ | 500 | 0 | 0 | 0.10 | 0.025 |
| A. | 该方应的正反应放热 | |
| B. | 达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大 | |
| C. | 达到平衡时,容器Ⅱ中c(H2)大于容器Ⅲ中c(H2)的两倍 | |
| D. | 达到平衡时,容器Ⅲ中的反应速率比容器Ⅰ中的大 |
| A. | 原子核内有10个中子的氧原子:${\;}_{6}^{18}$O | |
| B. | 氯原子的结构示意图: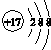 | |
| C. | Fe3+的最外层电子排布式为3s23p63d5 | |
| D. | 基态铜原子的外围电子排布图: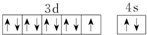 |
 ;ZX2的化学式是SiO2.
;ZX2的化学式是SiO2.