题目内容
在恒温和使用催化剂的条件下,向容积可变的密闭容器中,充入3mol H2和1mol N2,反应达到平衡时有a
mol NH3生成,N2的转化率为b%.
(1)若在相同条件下,向容积可变的密闭容器中充入x mol H2和y mol N2,反应达到平衡时有3a mol NH3生成,N2的转化率仍为b%,则x= ,y= .
(2)若在相同条件下,向容积可变的密闭容器中充入x mol H2、y mol N2和z mol NH3,若达到平衡时N2的转化率仍为b%,则x、y的关系为 ,z的取值范围为 .
(3)其他条件不变,向容积不变的密闭容器中充入3mol H2和1mol N2,反应达平衡时N2的转化率为c%,则b、c的大小关系是 .
mol NH3生成,N2的转化率为b%.
(1)若在相同条件下,向容积可变的密闭容器中充入x mol H2和y mol N2,反应达到平衡时有3a mol NH3生成,N2的转化率仍为b%,则x=
(2)若在相同条件下,向容积可变的密闭容器中充入x mol H2、y mol N2和z mol NH3,若达到平衡时N2的转化率仍为b%,则x、y的关系为
(3)其他条件不变,向容积不变的密闭容器中充入3mol H2和1mol N2,反应达平衡时N2的转化率为c%,则b、c的大小关系是
考点:等效平衡
专题:化学平衡专题
分析:(1)恒温恒压条件下,只要加入的起始的反应物的物质的量之比相同,就属于等效平衡,根据等效平衡知识计算出x、y;
(2)根据恒温恒压下的等效平衡分析x、y的关系及z的取值范围;
(3)根据在恒温恒容条件下,反应N2(g)+3H2(g)?2NH3(g),从起始到平衡状态时,反应的气体总物质的量减小,则压强减小分析.
(2)根据恒温恒压下的等效平衡分析x、y的关系及z的取值范围;
(3)根据在恒温恒容条件下,反应N2(g)+3H2(g)?2NH3(g),从起始到平衡状态时,反应的气体总物质的量减小,则压强减小分析.
解答:
解:(1)在恒温恒压下,由于氮气的转化率相同,该反应与原反应为等效平衡,由于反应达到平衡时有3amol NH3生成,说明加入的反应物的物质的量是原反应的各物质的物质的量的3倍,即加入了3mol×3=9mol氢气、1mol×3=3mol氮气,
故答案为:9;3;
(2)在恒温恒压下,氮气的转化率相同,所以该反应达到的平衡与原平衡互为等效平衡,由于初始加入的氮气和氢气满足化学分离式1:3的关系,所以氨气的物质的量不影响氮气的转化率,只要满足z≥0即可;而氮气和氢气的物质的量必须满足1:3,即x=3y,
故答案为:x=3y;z≥0;
(3)在恒温恒容条件下,由于该反应是气体体积减小的反应,从起始到平衡状态时,反应的气体总物质的量减小,则压强减小,不利于氨气的生成,所以生成的氨气的物质的量减小,氮气的转化率减小,即b>c,
故答案为:b大于c.
故答案为:9;3;
(2)在恒温恒压下,氮气的转化率相同,所以该反应达到的平衡与原平衡互为等效平衡,由于初始加入的氮气和氢气满足化学分离式1:3的关系,所以氨气的物质的量不影响氮气的转化率,只要满足z≥0即可;而氮气和氢气的物质的量必须满足1:3,即x=3y,
故答案为:x=3y;z≥0;
(3)在恒温恒容条件下,由于该反应是气体体积减小的反应,从起始到平衡状态时,反应的气体总物质的量减小,则压强减小,不利于氨气的生成,所以生成的氨气的物质的量减小,氮气的转化率减小,即b>c,
故答案为:b大于c.
点评:本题考查了化学平衡的计算,题目难度中等,涉及了等效平衡的判断及应用,注意恒温恒压条件下的等效平衡的条件,试题培养了学生的分析、理解、计算能力及灵活应用所学知识的能力.

练习册系列答案
相关题目
实验室将NaClO3和Na2SO3按物质的量之比1:2倒入烧瓶中,用水浴加热,同时滴入H2SO4,产生气体X,反应后测得NaClO3和Na2SO3恰好完全反应,则X为( )
| A、Cl2 |
| B、Cl2O |
| C、ClO2 |
| D、Cl2O3 |
富含维生素A的食物为( )
| A、动物肝脏 | B、水果 |
| C、谷物 | D、面包 |
下列实验装置设计正确且能达到相应实验目的是( )
A、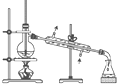 石油分馏 |
B、 制备乙酸乙酯 |
C、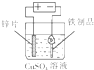 铁制品表面镀锌 |
D、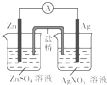 构成银锌原电池 |
下列电离方程式正确的是( )
| A、醋酸溶于水:CH3COOH=CH3COO-+H+ |
| B、熔融状态下的NaHSO4:NaHSO4=Na++H++SO42- |
| C、碳酸氢钠溶于水:HCO3-+H2O?CO32-+H3O+ |
| D、硫化氢溶于水:H2S?2H++S2- |
 某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度.
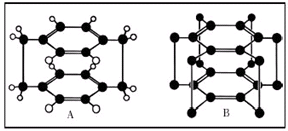
某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度.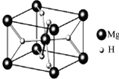 MgH2是金属氢化物储氢材料,其晶胞结构如图所示,已知该晶体的密度ag?cm-3,则晶胞的体积为
MgH2是金属氢化物储氢材料,其晶胞结构如图所示,已知该晶体的密度ag?cm-3,则晶胞的体积为
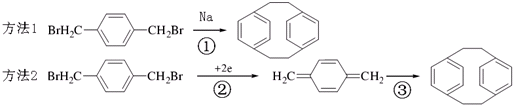 反应①的类型是:
反应①的类型是: