题目内容
14.工业制硫酸的过程中利用反应2SO2(g)+O2(g)$?_{△}^{催化剂}$2SO3(g);△H<0,将SO2转化为SO3,尾气SO2可用NaOH溶液进行吸收.请回答下列问题:(1)一定条件下,向一带活塞的密闭容器中充入2mol SO2和1mol O2发生反应,则下列说法正确的是DE
A.若反应速率v(SO2)﹦v(SO3),则可以说明该可逆反应已达到平衡状态
B.保持温度和容器体积不变,充入2mol N2,化学反应速率加快
C.平衡后仅增大反应物浓度,则平衡一定右移,各反应物的转化率一定都增大
D.平衡后移动活塞压缩气体,平衡时SO2、O2的百分含量减小,SO3的百分含量增大
E.保持温度和容器体积不变,平衡后再充入2mol SO3,再次平衡时SO2的百分含量比原平衡时SO2的百分含量小
F.平衡后升高温度,平衡常数K增大
(2)将一定量的SO2(g)和O2(g)分别通入到体积为2L的恒容密闭容器中,在不同温度下进行反应得到如表中的两组数据:
| 实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| SO2 | O2 | SO2 | O2 | |||
| 1 | T1 | 4 | 2 | x | 0.8 | 6 |
| 2 | T2 | 4 | 2 | 0.4 | y | 9 |
②T1>T2,(选填“>”、“<”或“=”),实验2中达平衡时 O2的转化率为90%;
(3)尾气SO2用NaOH溶液吸收后会生成Na2SO3.现有常温下0.1mol/L Na2SO3溶液,实验测定其pH约为8,完成下列问题:
①用离子方程式表示该溶液呈碱性的原因:SO32-+H2O?HSO3-+OH-;
②该溶液中c(OH-)=c(H+)+c(HSO3-)+2c(H2SO3)(用溶液中所含微粒的浓度表示).
(4)如果用含等物质的量溶质的下列各溶液分别来吸收SO2,则理论吸收量由多到少的顺序是B>C=D>A
A.Na2CO3 B.Ba(NO3)2 C.Na2S D.酸性KMnO4.
分析 (1)A.反应中正逆反应速率相同说明可逆反应已达到平衡状态;
B.保持温度和容器体积不变,加入与平衡无关的气体,总压增大,分压不变,化学反应速率不变;
C.平衡后仅增大反应物浓度,则平衡一定右移,另一种反应物的转化率一定增大,本身转化率减小;
D.平衡后移动活塞压缩气体,压强增大,平衡正向进行,平衡时SO2、O2的百分含量减小,SO3的百分含量增大;
E.保持温度和容器体积不变,平衡后再充入2molSO3,相当于增大压强,平衡正向进行;
F.反应是放热反应,平衡后升高温度,平衡逆向进行,平衡常数K减小;
(2)①分析图表数据,依据化学平衡三段式列式,结合反应速率概念计算;
②依据图表数据列式计算分析,反应 是放热反应,化学平衡随温度升高,平衡逆向进行分析两次实验的温度;
依据平衡三段式列式计算氧气的转化率;
(3)①常温下0.1mol/L Na2SO3溶液,实验测定其pH约为8,亚硫酸根离子水解溶液呈碱性;
②依据溶液中质子守恒分析书写离子浓度关系;
(4)依据选项中的溶液性质和二氧化硫反应的过程和化学方程式定量关系分析计算.
解答 解:(1)2SO2(g)+O2(g)$?_{△}^{催化剂}$2SO3(g)△H<0,反应是铜体积减小的放热反应,
A.反应速率之比等于化学方程式计量数之比,是正反应速率之比,反应速率v(SO2)=v(SO3),不能说明该可逆反应已达到平衡状态,故A错误;
B.保持温度和容器体积不变,充入2mol N2,加入与平衡无关的气体,总压增大,分压不变,化学反应速率不变,故B错误;
C.平衡后仅增大反应物浓度,则平衡一定右移,另一种反应物的转化率一定增大,加入的物质转化率减小,故C错误;
D.平衡后移动活塞压缩气体,压强增大,平衡正向进行,平衡时SO2、O2的百分含量减小,SO3的百分含量增大,故D正确;
E.保持温度和容器体积不变,平衡后再充入2molSO3,相当于增大压强,平衡正向进行,再次平衡时SO2的百分含量比原平衡时SO2的百分含量小,故E正确;
F.反应是放热反应,平衡后升高温度,平衡逆向进行,平衡常数K减小,故F错误;
故答案为:DE;
(2)①实验1从开始到反应达到化学平衡时,
2SO2(g)+O2(g)$?_{△}^{催化剂}$2SO3(g);
起始量(mol) 4 2 0
变化量(mol) 2.4 1.2 2.4
平衡量(mol) x 0.8 2.4
v(SO2)表示的反应速率=$\frac{\frac{2.4mol}{2L}}{6min}$=0.2mol/L•min;
故答案为:0.2 mol•L-1•min-1;
②依据反应起始量相同,达到平衡时氧气物质的量可知,实验2反应进行的程度大,反应是放热反应,温度越高,平衡向吸热反应方向进行,逆向进行,所以温度T1>T2,实验2中达平衡时 O2的转化率=$\frac{1.8mol}{2mol}$×100%=90%,故答案为:>;90%;
(3))①常温下0.1mol/L Na2SO3溶液,实验测定其pH约为8,亚硫酸根离子水解溶液呈碱性,水解反应方程式为:SO32-+H2O?HSO3-+OH-,故答案为:SO32-+H2O?HSO3-+OH-;
②常温下0.1mol/L Na2SO3溶液,该溶液中存在质子守恒,c(OH-)=c(H+)+c(HSO3-)+2c(H2SO3),故答案为:c(HSO3-)+2c(H2SO3);
(4)如果用含等物质的量溶质的下列各溶液分别来吸收SO2,则理论吸收量由多到少的顺序是
A.Na2CO3 吸收二氧化硫发生的反应为:Na2CO3+2SO2+H2O=2NaHSO3+CO2↑,1molNa2CO3 最多吸收二氧化硫2mol;
B.Ba(NO3)2 吸收二氧化硫反应化学方程式为Ba(NO3)2+3SO2+2H2O=BaSO4↓+2H2SO4+2NO↑:1molBa(NO3)2最多吸收二氧化硫3mol;
C.Na2S 吸收二氧化硫发生的反应为:2Na2S+5SO2+2H2O=4NaHSO3+3S↓,1mol2Na2S最多反应二氧化硫2.5mol;
D.酸性KMnO4溶液吸收二氧化硫的反应2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+,1molKMnO4最多反应二氧化硫2.5mol;
计算分析吸收二氧化硫理论吸收量由多到少的顺序是B>C=D>A,
故答案为:B>C=D>A.
点评 本题考查了化学平衡影响因素和平衡计算的分析判断,盐类水解分析应用,电解质溶液中离子浓度大小比较依据和方法,物质性质的理解应用,注意吸收二氧化硫的最大量反应判断,题目难度较大.

 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案| A. | CO32-+H2O?HCO3-+OH-:用热的纯碱溶液清洗油污 | |
| B. | A13++3H2O?AI(OH)3(胶体)+3H+:明矾净水 | |
| C. | SnCl2+H2O?Sn( OH)Cl↓+HCl配制氯化亚锡溶液时加入氢氧化钠溶液 | |
| D. | TiCl4+(x+2)H2O(过量)?TiO2•xH2O↓+3H+:制备TiO2纳米粉 |
2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ•mol-1,平衡时容器内气体压强为起始时的90%.保持同一反应温度,在相同容器中,将起始物质的量改为4mol SO2、3mol O2、2mol SO3(g),下列说法正确的是( )
| A. | 第一次实验平衡时反应放出的热量为294.9kJ | |
| B. | 两次实验平衡时,SO2的转化率相等 | |
| C. | 第二次实验达平衡时SO3的体积分数大于$\frac{2}{9}$ | |
| D. | 达平衡时,O2表示的反应速率为0.25mol/(L•min) |
(1)用CH4催化还原NO,可以消除氮氧化物的污染.已知:
①CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ•mol-1
②CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ•mol-1
由CH4将NO2完全还原成N2,生成CO2和水蒸气的热化学方程式是CH4(g)+2NO2(g)=CO2(g)+2H2O(g)+N2(g)△H=-867kJ•mol-1.
(2)NOx也可以被NaOH溶液吸收而生成NaNO3、NaNO2,已知某温度下,HNO2的电离常数K=-9.7×10-4,NO2-的水解常数K=-8.0×10-10,则该温度下水的离子积常数=Ka×Kh(用含Ka、Kb的代数式表示),此时溶液的温度>25℃(填“>”“<”或“=”).
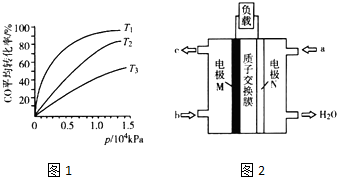
(3)化工上利用CO合成甲醇,反应的热化学方程式为CO(g)+2H2(g)?CH3OH(g)△H=-90.8kJ•mol-1.不同温度下,CO的平衡转化率与压强的关系如图1所示,图中T1、T2、T3的高低顺序是T1<T2<T3,理由是该反应为放热,温度越高,反应物的转化率越低.
(4)化工上还可以利用CH3OH生产CH3OCH3.在体积均为1.0L的恒容密闭容器中发生反应2CH3OH(g)?CH3OCH3(g)+H2O(g).
| 容器换号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
| CH3OH(g) | CH3OCH2(g) | H2O(g) | ||
| Ⅰ | 387 | 0.20 | 0.080 | 0.080 |
| Ⅱ | 207 | 0.20 | 0.090 | 0.090 |
(5)CH3OH燃料电池在便携式通讯设备、汽车等领域有着广泛的应用.已知电池工作时的总反应方程式为2CH3OH+3O2═2CO2+4H2O,电池工作时的示意图如图2所示.质子穿过交换膜移向N电极区(填“M”或“N”),负极的电极反应式为CH3OH+H2O-6e-=CO2+6H+.
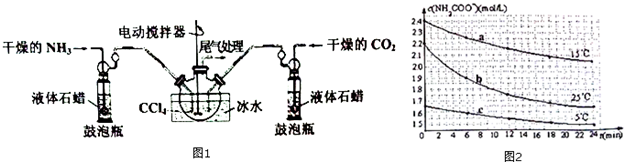
请回答下列问题:
(1)制备NH2COONH4的反应在一定条件下能自发进行,该反应的△H<0(填“>”“=”或“<”);要提高NH2COONH4的产率可采取的措施为增大压强、适当降低温度.
(2)装置中盛液体石蜡的鼓泡瓶作用是通过观察气泡,使气体流速均匀,调节NH3与CO2通入比例.
(3)一定条件下,在恒容密闭容器中通入体积比为2:1的NH3和CO2制备NH2COONH4固体.
①下列能说明反应达到平衡状态的是bd.
a、NH3和CO2物质的量之比为2:1
b.密闭容器中混合气体的密度不变
c、反应的焓变不变
d.固体的质量不在发生变化
②实验测得不同温度下达到平衡时气体的总浓度如表
| 温度(℃) | 20.0 | 30.0 | 40.0 |
| 平衡时气体总浓度 (×10-3mol•L-1) | 3.4 | 4.8 | 6.8 |
(4)己知:NH2C00NH4+2H20?NH4HCO3+NH3•H2O.分别用三份不份不同初始浓度的NH2COONH4溶液测定不同温度下的水解反应速率,得到c(NH2COO-)随时间变化趋势如图2所示.
①15℃时,0~6min内NH2COONH4水解反应的平均速率为0.05mol/(L•min).
②对比图中曲线a、b、c可知,水解反应速率最大的是b.
| A. | 通入稀有气体使压强增大,平衡将正向移动 | |
| B. | X的正反应速率是Y 的逆反应速率的$\frac{m}{n}$倍 | |
| C. | 降低温度,混合气体的平均相对分子质量变小 | |
| D. | 增加X的物质的量,平衡常数增大 |
| A. | 分解反应 | B. | 置换反应 | C. | 复分解反应 | D. | 化合反应 |