题目内容
在8HNO3+3Cu═3Cu(NO3)2+2NO↑+4H2O反应中,
(1)反应中氮元素 电子,化合价 ,被 ,作 剂;
(2) 是氧化产物, 是还原产物.
(3)在参加反应的硝酸中,起氧化剂作用的硝酸与起酸性作用的硝酸的质量比为 .当反应生成标况下22.4L气体时,转移 mol电子.
(4)在上述化学方程式中用双线桥表明电子转移的方向和数目.
(1)反应中氮元素
(2)
(3)在参加反应的硝酸中,起氧化剂作用的硝酸与起酸性作用的硝酸的质量比为
(4)在上述化学方程式中用双线桥表明电子转移的方向和数目.
考点:氧化还原反应
专题:氧化还原反应专题
分析:(1)氧化还原反应中失电子的元素化合价升高,得电子的元素化合价降低,化合价降低数目=化合价升高数目=转移的电子数目,;
(2)化合价降低元素所在的反应物是氧化剂,氧化剂反应的产物是还原产物,化合价升高元素所在的生成物是氧化产物;
(3)根据方程式计算判断,反应中N元素从+5降低到+2,则生成1molNO时,转移3mol电子;
(4)8HNO3(稀)+3Cu=3Cu(NO3)2+2NO↑+4H2O中,Cu元素的化合价由0升高为+2价,N元素的化合价由+5价降低为+2价,以此来解答.
(2)化合价降低元素所在的反应物是氧化剂,氧化剂反应的产物是还原产物,化合价升高元素所在的生成物是氧化产物;
(3)根据方程式计算判断,反应中N元素从+5降低到+2,则生成1molNO时,转移3mol电子;
(4)8HNO3(稀)+3Cu=3Cu(NO3)2+2NO↑+4H2O中,Cu元素的化合价由0升高为+2价,N元素的化合价由+5价降低为+2价,以此来解答.
解答:
解:(1)反应中N元素得电子化合价降低,HNO3为氧化剂,Cu元素化合价升高,被氧化,根据方程式可判断,当8molHNO3参加反应时,有2mol被还原,表现为氧化性,6molHNO3表现为酸性,被还原的HNO3与参加反应的HNO3物质的量之比是1:4;反应中硝酸作氧化剂,表现了氧化性,反应生成硝酸铜还表现了硝酸的酸性;
故答案为:得;降低;还原;氧化;
(2)化合价降低元素所在的反应物是氧化剂,氧化剂反应的产物是还原产物,则NO为氧化产物;
故答案为:Cu(NO3)2;NO;
(3)在参加反应的硝酸中,化合价降低的部分起氧化剂作用的数目为2,起酸性作用的硝酸的数目为6,则其质量比为1:3;反应中N元素从+5降低到+2,则生成1molNO时,转移3mol电子,则当反应生成标况下22.4L气体,即1mol气体时,转移3mol电子;
故答案为:1:3;3;
(4)Cu元素的化合价由0升高为+2价,N元素的化合价由+5价降低为+2价,则用双线桥标明电子转移的方向和数目为 ,
,
故答案为: .
.
故答案为:得;降低;还原;氧化;
(2)化合价降低元素所在的反应物是氧化剂,氧化剂反应的产物是还原产物,则NO为氧化产物;
故答案为:Cu(NO3)2;NO;
(3)在参加反应的硝酸中,化合价降低的部分起氧化剂作用的数目为2,起酸性作用的硝酸的数目为6,则其质量比为1:3;反应中N元素从+5降低到+2,则生成1molNO时,转移3mol电子,则当反应生成标况下22.4L气体,即1mol气体时,转移3mol电子;
故答案为:1:3;3;
(4)Cu元素的化合价由0升高为+2价,N元素的化合价由+5价降低为+2价,则用双线桥标明电子转移的方向和数目为
 ,
,故答案为:
 .
.
点评:本题考查氧化还原反应,为高考常见考点,明确反应中元素的化合价变化是解答的关键,侧重基本概念和转移电子数的考查,题目难度不大.

练习册系列答案
相关题目
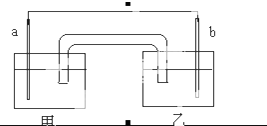 某化学兴趣小组设计如图原电池:其中a、b分别为Cu和Ag,甲和乙分别是氨水和硝酸银溶液,盐桥的琼脂中吸附有KCl溶液,反应一段时间后,下列说法正确的是( )
某化学兴趣小组设计如图原电池:其中a、b分别为Cu和Ag,甲和乙分别是氨水和硝酸银溶液,盐桥的琼脂中吸附有KCl溶液,反应一段时间后,下列说法正确的是( )| A、b为负极,电极方程式为:Ag++e-═Ag |
| B、甲中出现大量蓝色沉淀 |
| C、总反应为:Cu+2Ag+═Cu2++Ag |
| D、反应时,盐桥中的K+向乙方向移动 |
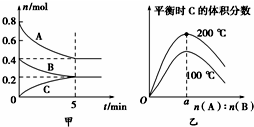 在2L的密闭容器中发生反应xA(g)+yB(g)?zC(g).图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系.则下列结论正确的是( )
在2L的密闭容器中发生反应xA(g)+yB(g)?zC(g).图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系.则下列结论正确的是( )| A、200℃时,反应从开始到平衡的平均速率v(B)=0.04 mol?L-1?min-1 |
| B、200℃时,该反应的平衡常数为25 L2/mol2 |
| C、当外界条件由200℃降温到100℃,原平衡一定被破坏,且正逆反应速率均增大 |
| D、由图乙可知,反应xA(g)+yB(g)?zC(g)的△H<0,且a=2 |
 2013年9月,中国华北华中地区发生了严重的雾霆天气,北京、河北、河南等地的空气污染升为6级空气污染,属于重度污染.汽车尾气、燃煤废气、冬季取暖排放的CO2等都是雾霆形成的原因.
2013年9月,中国华北华中地区发生了严重的雾霆天气,北京、河北、河南等地的空气污染升为6级空气污染,属于重度污染.汽车尾气、燃煤废气、冬季取暖排放的CO2等都是雾霆形成的原因.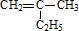 的键线式
的键线式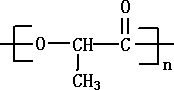 是由一种单体缩聚而成的,该单体的结构简式为
是由一种单体缩聚而成的,该单体的结构简式为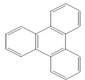 的一氯取代物有
的一氯取代物有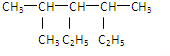
 分子中含氧官能团的名称是
分子中含氧官能团的名称是