题目内容
下列对实验现象的解释与结论正确的是( )
| 编号 | 实验操作 | 实验现象 | 解释与结论 |
| A | 向某溶液中加入AgNO3溶液 | 有白色沉淀产生 | 生成了难溶于水的AgCl, 该溶液中一定含有Cl- |
| B | 向鸡蛋清溶液中, 加入饱和(NH4)2SO4溶液 | 有白色沉淀产生 | 蛋白质发生了盐析 |
| C | 向甲苯中滴入少量浓溴水,振荡,静置 | 溶液分层,上层呈橙红色,下层几乎无色 | 甲苯和溴水发生取代反应, 使溴水褪色 |
| D | 向蔗糖中加入浓硫酸 | 变黑,放热,体积膨胀,放出刺激性气体 | 浓硫酸具有吸水性和强氧化性, 反应中生成C、SO2和CO2等 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:
分析:A.能和AgNO3溶液反应生成白色沉淀的离子有Ag+、SO42-、CO32-等;
B.饱和(NH4)2SO4溶液能使蛋白质溶解度减小而发生盐析;
C.溴在甲苯中的溶解度大于水中的溶解度,甲苯和溴不反应,且甲苯和水不互溶;
D.浓硫酸具有脱水性,能将蔗糖中的H、O元素以水的形式脱去.
B.饱和(NH4)2SO4溶液能使蛋白质溶解度减小而发生盐析;
C.溴在甲苯中的溶解度大于水中的溶解度,甲苯和溴不反应,且甲苯和水不互溶;
D.浓硫酸具有脱水性,能将蔗糖中的H、O元素以水的形式脱去.
解答:
解:A.能和AgNO3溶液反应生成白色沉淀的离子有Ag+、SO42-、CO32-等,所以向某溶液中加入AgNO3溶液产生白色沉淀,不能说明原来溶液中含有Cl-,故A错误;
B.饱和(NH4)2SO4溶液能使蛋白质溶解度减小而发生盐析,所以向鸡蛋清溶液中,加入饱和(NH4)2SO4溶液,有白色沉淀生成,盐析具有可逆性,故B正确;
C.溴在甲苯中的溶解度大于水中的溶解度,甲苯和溴不反应,且甲苯和水不互溶,所以甲苯能作溴的萃取剂,向甲苯中滴入少量浓溴水,振荡,静置,溶液分层,上层呈橙红色,下层几乎无色,发生了萃取而使溴水褪色,故C错误;
D.浓硫酸具有脱水性,能将蔗糖中的H、O元素以水的形式脱去,向蔗糖中加入浓硫酸,蔗糖变黑,放热,体积膨胀,放出刺激性气体,浓硫酸体现氧化性和脱水性,故D错误;
故选B.
B.饱和(NH4)2SO4溶液能使蛋白质溶解度减小而发生盐析,所以向鸡蛋清溶液中,加入饱和(NH4)2SO4溶液,有白色沉淀生成,盐析具有可逆性,故B正确;
C.溴在甲苯中的溶解度大于水中的溶解度,甲苯和溴不反应,且甲苯和水不互溶,所以甲苯能作溴的萃取剂,向甲苯中滴入少量浓溴水,振荡,静置,溶液分层,上层呈橙红色,下层几乎无色,发生了萃取而使溴水褪色,故C错误;
D.浓硫酸具有脱水性,能将蔗糖中的H、O元素以水的形式脱去,向蔗糖中加入浓硫酸,蔗糖变黑,放热,体积膨胀,放出刺激性气体,浓硫酸体现氧化性和脱水性,故D错误;
故选B.
点评:本题考查化学实验方案评价,涉及离子检验、盐析、萃取、浓硫酸的性质等知识点,侧重考查学生实验操作、分析问题能力,注意盐析和变性、吸水性和脱水性等区别,知道萃取剂的选取方法,题目难度不大.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
下列物质属于电解质的是( )
| A、CO2 |
| B、Cl2 |
| C、BaSO4 |
| D、NaOH溶液 |
设NA是阿伏加德罗常数的值,下列说法正确的是( )
| A、在32 g18O2中含有2NA个氧原子 |
| B、1molCl2与足量的铁反应转移的电子数与1mol铁与足量的Cl2反应转移的电子数相等 |
| C、某温度下纯水的pH=6,该温度下10LpH=11的NaOH溶液中含OH-的数目为NA |
| D、一定条件下,将1 mol N2与3 mol H2混合反应后,生成NH3分子的数目为2NA |
对化学用语的理解影响我们的学习,下列叙述正确的是( )
| A、氯化钠溶液在电流作用下电离成氯离子和钠离子 |
| B、溶于水后电离出氢离子的化合物都是酸 |
| C、硫酸钡难溶于水但硫酸钡是强电解质 |
| D、氨气溶于水能部分电离,故氨气属于弱电解质 |
 如图是有关“水”部分知识的网络图(反应条件已省略),用化学用语填空:
如图是有关“水”部分知识的网络图(反应条件已省略),用化学用语填空: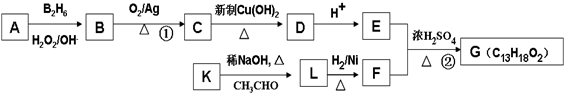

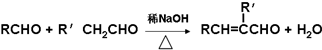
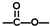 ”结构的共有
”结构的共有
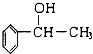 )互为同系物.
)互为同系物.