题目内容
11.硫化钠主要用于皮革、毛纺、高档纸张、染料等行业.生产硫化钠大多采用无水芒硝(Na2SO4)-炭粉还原法,其流程示意图如图1: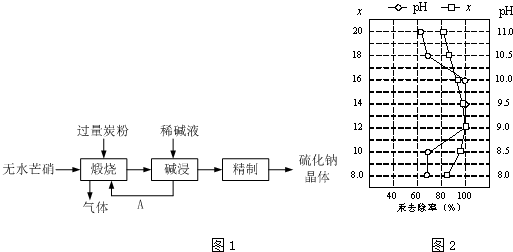
(1)上述流程中“碱浸”后,物质A必须经过过滤、干燥(填写操作名称)处理后,方可“煅烧”;若煅烧所得气体为等物质的量的CO和CO2,写出煅烧时发生的总的化学反应方程式为3Na2SO4+8C$\frac{\underline{\;高温\;}}{\;}$3Na2S+4CO2↑+4CO↑.
(2)上述流程中采用稀碱液比用热水更好,理由是稀碱液能抑制Na2S水解(选促进或抑制)
(3)取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌.若反应后测得溶液的pH=4,则此时溶液中c( S2-)=4×10-36 mol•L-1.(已知:常温时CuS、Cu(OH)2的Ksp分别为8.8×10-36、2.2×10-20)
(4)①皮革工业废水中的汞常用硫化钠除去,汞的去除率与溶液的pH和x(x代表硫化钠的实际用量与理论用量的比值)有关(如图2所示).为使除汞效果最佳,应控制的条件是x控制x=12、pH控制pH介于9~10之间.
②某毛纺厂废水中含0.001mol•L-1的硫化钠,与纸张漂白后的废水(含0.002mol•L-1 NaClO)按1:2的体积比混合,能同时较好处理两种废水,处理后的废水中所含的主要阴离子有SO42-、Cl-.
分析 根据图1可知,制备硫化钠晶体的流程为:无水芒硝(Na2SO4)与碳在高温煅烧反应:3Na2SO4+8C$\frac{\underline{\;高温\;}}{\;}$3Na2S+4CO2↑+4CO↑,由于硫离子水解,则用稀碱溶液浸泡抑制硫离子水解,通过精制获得硫化钠晶体,
(1)从获得固体A的原混合物状态分析操作方法,由于煅烧时加入过量的炭粉,且固体A可以分离并进行煅烧的应用分析A是什么物质;依据题干信息可知生成物中除含有硫化钠外还含有一氧化碳和二氧化碳,以及两种碳的氧化物分子个数比是1:1进行分析判断即可;
(2)依据硫化钠溶液中硫离子水解显碱性的水解平衡影响因素分析判断;
(3)常温时CuS、Cu(OH)2的Ksp,依据溶度积常数计算得到,依据溶液PH计算溶液中铜离子浓度,依据CuS的Ksp计算得到硫离子的浓度;
(4)①依据图象中曲线分析,汞去除率最佳PH和x的取值;
②依据硫化钠和次氯酸钠在溶液中发生的氧化还原反应电子守恒计算分析判断.
解答 解:(1)由于固体A是从液体中获得,所以得到A的操作是过滤,由于煅烧时加入过量的炭粉,且固体A可以分离并进行煅烧的应用可知A是炭粉,化学式为C;从题干信息可知生成物中除含有硫化钠外还含有一氧化碳和二氧化碳,而反应物是硫酸钠和碳,根据煅烧时一氧化碳和二氧化碳的分子个数比是1:1,所以可设两种气体的化学计量数分别是1和1,可得该反应的方程式为:$\frac{3}{4}$Na2SO4+2C $\frac{\underline{\;高温\;}}{\;}$$\frac{3}{4}$Na2S+1CO2↑+1CO↑,该反应两边同乘以4所得的反应方程式为:3Na2SO4+8C$\frac{\underline{\;高温\;}}{\;}$3Na2S+4CO2↑+4CO↑,
故答案为:过滤、干燥;3Na2SO4+8C$\frac{\underline{\;高温\;}}{\;}$3Na2S+4CO2↑+4CO↑;
(2)上述流程中采用稀碱液比用热水更好,硫化钠溶液中硫离子水解显碱性,水解过程是吸热反应,加热促进水解进行,稀碱溶液能起到抑制水解的作用,
故答案为:抑制;
(3)取硫化钠晶体(含少量NaOH)加入到硫酸铜溶液中,充分搅拌.若反应后测得溶液的pH=4,常温时CuS、Cu(OH)2的Ksp分别为8.8×10-36、2.2×10-20,
Ksp=c(Cu2+)×c2(OH-)=2.2×10-20,pH=4,c(OH-)=10-10mol/L,c(Cu2+)=2.2mol/L,硫化铜中的Ksp=c(Cu2+)c(S2-)=8.8×10-36、计算得到c(S2-)=4×10-36mol/L,
故答案为:4×10-36;
(4)①依据图象中曲线分析,汞去除率最佳PH和x的取值是x=12,pH介于9~10之间时汞的去除率最大,接近100%,
故答案为:x=12、pH介于9~10之间;
②某毛纺厂废水中含0.001mol•L-1的硫化钠,与纸张漂白后的废水(含0.002mol•L-1 NaClO)按1:2的体积比混合,能同时较好处理两种废水,次氯酸钠和硫化钠发生氧化还原反应,n(Na2S):n(NaClO)=0.001mol/L×1:0.002mol•L-1×2=1:4,依据电子守恒分析可知,Na2S+4NaClO=Na2SO4+4NaCl,处理后的废水中所含的主要阴离子有SO42-、Cl-,
故答案为:SO42-、Cl-.
点评 本题是物质制备的考查题,主要是化学方程式书写方法,溶度积常数的计算分析,氧化还原反应电子守恒的计算应用,掌握基础是关键,题目难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 两种物质反应,不管怎样书写化学方程式,平衡常数不变 | |
| B. | 某温度下,2L密闭容器中加入4mol A和2mol B发生反应: 3A(g)+2B(g)?4C(s)+2D(g).平衡时测得n(C)=1.6mol,反应的化学平衡常数表达式为K=$\frac{{c}^{4}(C){c}^{2}(D)}{{c}^{3}(A){c}^{2}(B)}$ | |
| C. | 温度一定时,当溶液中c(Ag+)•c(Cl-)等于Ksp值时,此溶液为AgCl的饱和溶液 | |
| D. | 难溶电解质AB2饱和溶液中,c(A2+)=x mol•L-1,c(B-)=y mol•L-1,则Ksp值为4xy2 |
| 化学键 | H-H | N三N | N-H |
| 键能/(kJ•mol-1) | 436 | 945.6 | 391 |
| A. | +192.4 kJ•mol-1 | B. | +92.4kJ•mol-1 | C. | -92.4kJ•mol-1 | D. | -192.4kJ•mol-1 |
(一)鉴别NaCl和NaNO2
甲同学用沉淀分析法
经查:常温下Ksp(AgNO2)=2×10-8,Ksp(AgCl)=1.8×10-10.分别向盛有5mL 0.0001mol/L两种盐溶液的试管中同时逐滴滴加0.0001mol/L硝酸银溶液,先生成沉淀的是盛有NaCl溶液的试管.
乙同学测定溶液pH
用pH试纸分别测定0.1mol/L两种盐溶液的pH,测得NaNO2溶液呈碱性.该溶液呈碱性的原因是NO2-+H2O?HNO2+OH-(用离子方程式解释).
(二)该小组用如下装置(略去夹持仪器)制备亚硝酸钠
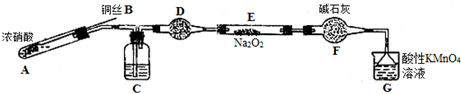
已知:①2NO+Na2O2=2NaNO2;
②酸性条件下,NO和NO2都能与MnO4- 反应生成NO3-和Mn2+
(1)使用铜丝的优点是可以控制反应的发生与停止.
(2)装置A中反应方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O.装置C 中盛放的药品是C;(填字母代号)
A.浓硫酸 B.NaOH 溶液 C.水 D.四氯化碳
仪器F的作用防止水蒸气进入.
(3)该小组称取5.000g制取的样品溶于水配成250.0mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol/L酸性KMnO4溶液进行滴定,实验所得数据如下表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| 消耗KMnO4溶液体积/mL | 20.70 | 20.12 | 20.00 | 19.88 |
a.锥形瓶洗净后未干燥
b.酸式滴定管用蒸馏水洗净后未用标准液润洗
c.滴定终点时仰视读数
②酸性KMnO4溶液滴定亚硝酸钠溶液的离子方程式为6H++2MnO4-+5NO2-=2Mn2++5NO3-+3H2O.
③该样品中亚硝酸钠的质量分数为69.0%.
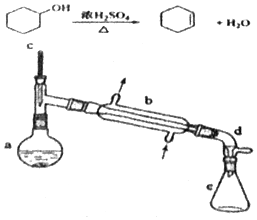 分离提纯是化学实验中的重要部分,方法有过滤、蒸发、萃取、蒸馏等,应用广泛,环己醇 脱水是合成环己烯的常用方法,实验室合成坏己烯的反应和实验装置如图:
分离提纯是化学实验中的重要部分,方法有过滤、蒸发、萃取、蒸馏等,应用广泛,环己醇 脱水是合成环己烯的常用方法,实验室合成坏己烯的反应和实验装置如图:可能用到的有关数据如下:
| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1ml浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃.
Ⅱ.分离提纯:
反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯10g.
回答下列问题:
(1)装置b的名称是冷凝管.
(2)加入碎瓷片的作用是防止暴沸;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)分液漏斗在使用前须清洗干净并检漏;在本实验分离过程中,产物应该从分液漏斗的上口倒出(填“上口倒出”或“下口倒出”).
(4)分离提纯过程中加入无水氯化钙的目的是干燥.
(5)在环己烯粗产物蒸馏过程中,不可能用到的仪器有C(填正确答案标号).
A.蒸馏烧瓶 B.温度计 C.分液漏斗 D.牛角管 E.锥形瓶.
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H2=-57.3kJ/mol.
下列结论正确的是( )
| A. | 碳的燃烧热为221KJ/mol | |
| B. | 稀盐酸与稀NaOH溶液反应生成1mol水,放出的热量57.3KJ | |
| C. | 浓硫酸与稀NaOH溶液反应的中和热值为57.3KJ/mol | |
| D. | 稀醋酸与稀NaOH溶液反应生成1mol水,放出的热量57.3KJ |
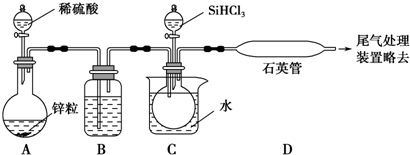
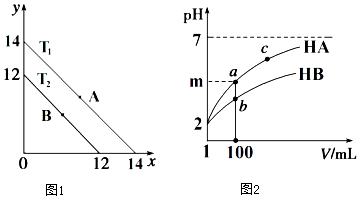 (1)溶液中,c(H+)=10-x mol•L-1,c(OH-)=10-y mol•L-1,x与y的关系如图1所示.
(1)溶液中,c(H+)=10-x mol•L-1,c(OH-)=10-y mol•L-1,x与y的关系如图1所示.