��Ŀ����
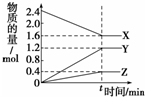
1����I����һ���ݻ�Ϊ2L���ܱ������У�����1mol SO2��1mol O2��һ�������·�����Ӧ2SO2+O2?2SO3��3���Ӻ���SO3�����ʵ���Ϊ0.6mol�����ʱO2�����ʵ���Ũ��Ϊ0.15mol/L����SO2��ʾ�Ļ�ѧ��Ӧ������0.1mol/��L��min������II����2L��������3�����ʽ��з�Ӧ��X��Y��Z�����ʵ�����ʱ��ı仯������ͼ��ʾ����Ӧ��tʱ�̴ﵽƽ��
��1���÷�Ӧ�Ļ�ѧ����ʽ��2X?3Y+Z��
��2����t=10ʱ����Ӧ��ʼ��tʱ�̣�Y��ƽ����Ӧ������0.02mol/��L��min����
��3�����ڸ÷�Ӧ��˵����ȷ����BC��
A������tʱ�̸÷�Ӧ��ֹͣ
B����tʱ��֮ǰX���������ʴ���������������
C����tʱ������Ӧ���ʵ����淴Ӧ����
D����tʱ�̴ﵽƽ������Ϊ��ʱ��Ӧ�������ʵ����������������ʵ�����ȣ�
���� ��I�� 2SO2+O2?2SO3��
��ʼ��mol��1 1 0
��Ӧ��mol��0.6 0.3 0.6
3min��mol��0.4 0.7 0.6
c��O2��=$\frac{��n}{V}$��v��SO2��=$\frac{\frac{��n}{V}}{��t}$��
��II����1�����ŷ�Ӧ�Ľ��У�X�����ʵ������٣�Y��Z�����ʵ������ӣ���X�Ƿ�Ӧ�Y��Z��������ﵽƽ��ʱ��n��X��=��2.4-1.6��mol=0.8mol����n��Y��=��1.2-0��mol=1.2mol����n��Z��=��0.4-0��mol=0.4mol��ͬһ���淴Ӧ�У�ͬһ��ʱ���ڣ��μӷ�Ӧ�ĸ����ʵ����ʵ����仯��֮�ȵ����������֮�ȣ�
��2��v��Y��=$\frac{\frac{��n}{V}}{��t}$��
��3����Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ���Ӧ���ڶ�̬ƽ��״̬����Ӧ��ϵ�и����ʵ����ʵ������䣮
��� �⣺��I�� 2SO2+O2?2SO3��
��ʼ��mol��1 1 0
��Ӧ��mol��0.6 0.3 0.6
3min��mol��0.4 0.7 0.6
c��O2��=$\frac{��n}{V}$=$\frac{0.3mol}{2L}$=0.15mol/L��v��SO2��=$\frac{\frac{��n}{V}}{��t}$=$\frac{\frac{0.6mol}{2L}}{3min}$=0.1mol/��L��min����
�ʴ�Ϊ��0.15mol/L��0.1mol/��L��min����
��II����1�����ŷ�Ӧ�Ľ��У�X�����ʵ������٣�Y��Z�����ʵ������ӣ���X�Ƿ�Ӧ�Y��Z��������ﵽƽ��ʱ��n��X��=��2.4-1.6��mol=0.8mol����n��Y��=��1.2-0��mol=1.2mol����n��Z��=��0.4-0��mol=0.4mol��ͬһ���淴Ӧ�У�ͬһ��ʱ���ڣ��μӷ�Ӧ�ĸ����ʵ����ʵ����仯��֮�ȵ����������֮�ȣ���X��Y��Z�ļ�����֮��=0.8mol��1.2mol��0.4mol=2��3��1����÷�Ӧ����ʽΪ2X?3Y+Z��
�ʴ�Ϊ��2X?3Y+Z��
��2��v��Y��=$\frac{\frac{��n}{V}}{��t}$=$\frac{\frac{1.2mol}{2L}}{10min}$=0.02mol/��L��min�����ʴ�Ϊ��0.02mol/��L��min����
��3��A������tʱ�̣����淴Ӧ������ȣ���Ӧ���ڶ�̬ƽ��״̬����A����
B����tʱ��֮ǰƽ�������ƶ�����X���������ʴ��������������ʣ���B��ȷ��
C����tʱ�̷�Ӧ����ƽ��״̬������Ӧ���ʵ����淴Ӧ���ʣ���C��ȷ��
D����tʱ�̴ﵽƽ�������淴Ӧ������ȣ���Ӧ��ϵ�и����ʵ����ʵ������䣬����Ӧ������ʵ�����һ������������������ʵ������뷴Ӧ��ʼ���ʵ�����ת�����йأ���D����
��ѡBC��
���� ���⿼�黯ѧƽ����㼰��ѧƽ��״̬�жϣ�Ϊ��Ƶ���㣬���ؿ���ѧ�������жϼ�������������ȷƽ��״̬��������ѧƽ������еġ�����ʽ���ǽⱾ��ؼ�����Ŀ�ѶȲ���

| A�� | FeCl3�TFe3++Cl3- | B�� | NaHCO3�TNa++H++CO32- | ||
| C�� | Al2��SO4��3�T2Al3++3SO42- | D�� | KMnO4�TK++Mn7++4O2- |
| A�� | ������ˮ | B�� | ͨHCl���� | C�� | ��NaOH���� | D�� | ��MgSO4 ���� |
��1����֪��CH3OH��l��+$\frac{3}{2}$O2��g���TCO2��g��+2H2O��l����H=-725.5kJ•mol-1
��H2��g��+$\frac{1}{2}$O2��g���TH2O��g����H=-241.8kJ•mol-1
��H2O��g���TH2O��l����H=-44kJ•mol-1
��ҵ����CO2��g����H2��g��Ϊԭ�Ϻϳ�CH3OH��l����ͬʱ����H2O��l�����Ȼ�ѧ����ʽΪCO2��g��+3H2��g���TCH3OH��l��+H2O��l����H=-131.9kJ•mol-1��
��2����CO2ת��Ϊ���ѵķ�Ӧԭ��Ϊ2CO2��g��+6H2��g��?CH3OCH3��g��+3H2O��l��
��֪��Ͷ�ϱ�n��CO2����n��H2��=1��3�������£���ͬ�¶ȡ���ͬѹǿʱ��CO2��ת���ʼ�����
| �¶� ת���� ѹǿ | 500K | 600K |
| P | 60% | b |
| 1.5P | a | 55% |
A���ں��¡����ݵ��ܱ������У�����Ӧ���������ܶȱ��ֲ���ʱ��Ӧ��ƽ��״̬
B����v����CO2��=3v����H2������Ӧ��ƽ��״̬
C����n��CO2����n��H2��=1��3ʱ����Ӧ��ƽ��״̬
D��a��60%
��������Ӧ�Ļ�ѧƽ�ⳣ���ı���ʽΪK=$\frac{c��C{H}_{3}OC{H}_{3}��}{{c}^{2}��C{O}_{2}����{c}^{6}��{H}_{2}��}$��
�۸÷�Ӧ�ġ�H��0��ԭ�����ɱ������ݿ��ж�b��55%���ɵ��¶����ߣ���Ӧ��ת���ʽ��ͣ���������Ӧ���ȣ�
����ѹǿΪP���¶�Ϊ500K��Ͷ�ϱ�n��CO2����n��H2��=1��3�������£���Ӧ��ƽ��״̬ʱH2��ת����Ϊ60%�����������CO2���������Ϊ$\frac{4}{19}$��
��3���Լ״���������KOH��ҺΪԭ�Ͽ���Ƴ�ȼ�ϵ�أ��ŵ�ʱ�������ĵ缫��ӦʽΪCH3OH-8e-+8OH-=CO32-+6H2O��
| A�� | 10g H2 | B�� | 2molCl2 | C�� | 1.5NACO2 | D�� | 22.4LO2����״���� |
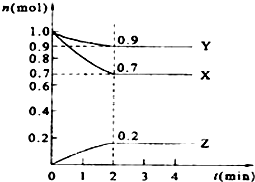 ij�¶�ʱ����2L���ܱ������У�X��Y��Z�������ʵ�����ʱ��ı仯������ͼ��ʾ��
ij�¶�ʱ����2L���ܱ������У�X��Y��Z�������ʵ�����ʱ��ı仯������ͼ��ʾ�� ��������һ����Ҫ���л�����ԭ�ϣ���е�Ϊ38.4�森�Ʊ��������һ�ַ������Ҵ��������ᷴӦ���÷�Ӧ�Ļ�ѧ����ʽ��CH3CH2OH+HBr$��_{��}^{Ũ����}$CH3CH2Br+H2O��
��������һ����Ҫ���л�����ԭ�ϣ���е�Ϊ38.4�森�Ʊ��������һ�ַ������Ҵ��������ᷴӦ���÷�Ӧ�Ļ�ѧ����ʽ��CH3CH2OH+HBr$��_{��}^{Ũ����}$CH3CH2Br+H2O��