题目内容
(08枣庄调研)某课外活动小组用如图所示的实验装置探究氯气与氨气之间的反应。其中A、F为氨气和氯气的发生装置,C为纯净、干燥的氯气与氨气反应的装置。
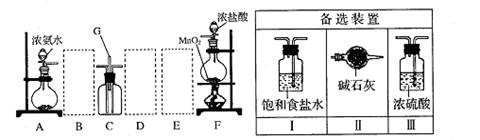
请回答下列问题:
(1)装置F中发生反应的离子方程式是 。
(2)装置A中的烧瓶内固体可选用 (选填以下选项的代号)。
A.碱石灰 B.浓硫酸 C.生石灰 D.五氧化二磷 E.烧碱
(3)虚线框内应添加必要的除杂装置,请从右图的备选装置中选择,并将编号填入下列空格。B 、D 、E 。
(4)氯气和氨气在常温下混合就能发生反应生成氯化铵和氮气,该反应的化学方程式为: ;装置C内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案鉴定该固体就是氯化铵: 。
(5)若从装置C和G处逸出的尾气中含有N2和少量C12,应如何处理?
答案:
(1)MnO2+4H++2C1- Mn2++C12↑+2H2O(2分)
(2)A C D(3分,漏一项扣1分,错一项扣2分。)
(3)Ⅱ(1分) Ⅲ(1分)Ⅰ(1分)
(4)8NH3+3C12 6NH4C1+N2(2分)
将固体在烧杯中溶解,用试管取少量溶液,然后滴加少量硝酸酸化的AgNO3溶液,有白色沉淀产生,证明有C1-;用试管取秒量溶液,加入浓烧碱溶液,加热,再将湿润的红色石蕊试纸放在试管口,红色石蕊试纸变蓝证明有NH4+
(5)将导气管与GO连接,另一端插入盛有NaOH溶液的烧杯中(1分)

 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案(08枣庄调研)学习元素周期律后,某研究性学习小组的同学们对第四周期过渡元素的氧化物产生了浓厚的兴趣。在已知二氧化锰对氯酸钾催化分解知识的基础上,联想到氧化铁、氧化铜、氧化铬等对氯酸钾的分解是否有催化作用,对此他们进行了实验研究。
请根据要求完成下列部分实验报告:
(1)课题名称: 。
(2)实验仪器及试剂:
实验仪器:带铁夹的铁架台、带橡皮塞的导管、量气装置、过滤装置、电子天平、药匙、等。
实验试剂:二氧化锰、氧化铁、氧化铜、氧化铬和氯酸钾
(3)实验步骤:略
(4)实验数据:
实验 编号 | KC1O3/g | 氧化物 | 产生气体/mL (已折算到标况) | 耗时/s | ||
化学式 | 质量/g | 回收 | ||||
1 | 0.60 | ― | ― | ― | 10 | 480 |
2 | 0.60 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
3 | 0.60 | CuO | 0.20 | 90% | 67.2 | 79.5 |
4 | 0.60 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
5 | 0.60 | Cr2O3 | 0.20 | 90% | 67.2 | 188.3 |
(5)实验讨论:
①在氧化物的回放过程中,要进行的操作是溶解、 、洗涤、 、称量。
②实验编号3的实验中KC1O3的分解率为 (保留一位小数)。
③在和Cr2O3做研究实验时,发现有刺激性气味的气体产生,同时绿色的混合物变成了橘黄色。该刺激性气味的气体是 ,可用 试纸检验。上述异常现象产生的原因是 。
(6)实验结论 。