题目内容
19.利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如下: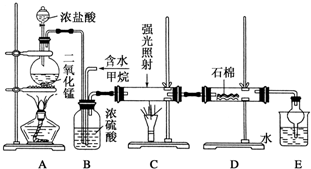
根据设计要求回答:
(1)A装置中发生反应的离子方程式是MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O
(2)B装置有三种功能:①控制气流速度;②均匀混合气体;③干燥混合气体.
(3)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式:CH4+2Cl2$\stackrel{强光}{→}$C+4HCl.
(4)D装置的石棉中均匀混有KI粉末,其作用是:吸收过量的氯气.
(5)E装置除生成盐酸外,还含有有机物,从E中分离出盐酸的最佳方法为分液.
分析 (1)二氧化锰与浓盐酸在加热条件下反应生成氯气、氯化锰和水;
(2)装置有三种功能:①控制气流速度;②均匀混合气体;③干燥混合气体干燥混合气体;
(3)依据题意:在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,可知甲烷与氯气在强光下反应生成碳和氯化氢;
(4)氯气能将碘化钾氧化为碘单质;
(5)最后生成的HCl溶于水生成盐酸,与有机物可用分液的方法分离.
解答 解:(1)二氧化锰与浓盐酸在加热条件下反应生成氯气、氯化锰和水,离子方程式:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
(2)装置有三种功能:①控制气流速度;②均匀混合气体;③干燥混合气体干燥混合气体;
故答案为:控制气流速度;
(3)甲烷与氯气在强光下反应生成碳和氯化氢,化学方程式:CH4+2Cl2$\stackrel{强光}{→}$C+4HCl;
故答案为:CH4+2Cl2$\stackrel{强光}{→}$C+4HCl;
(4)氯气具有氧化性,KI中-1价的碘能被氯气氧化,产物为氯化钾固体和碘单质,所以,D装置的石棉中均匀混有KI粉末,能吸收过量的氯气,
故答案为:吸收过量的氯气;
(5)E装置中除了有盐酸生成外,还含有二氯甲烷、三氯甲烷和四氯化碳,二氯甲烷、三氯甲烷和四氯化碳不溶于水,能分层,可用分液分开;
故答案为:分液.
点评 本题考查氯气的制备以及甲烷与氯气的取代反应,题目难度中等,本题注意把握题给信息,注意把握产物的判断.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
9.现有A、B、C、D四种短周期非金属元素,它们的原子最外层电子数之和为19.在它们的化合物中,主要化合价均不止一种,但有一种相同的化合价.它们的部分性质如下:
(1)A元素在元素周期表中的位置为第三周期ⅥA族.
(2)含D元素的两种常见共价化合物发生化合反应可生成一种离子化合物,该反应的化学方程式为NH3+HNO3═NH4NO3.
(3)B的单质与D的最高价氧化物对应的水化物在加热条件下发生反应的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑+CO2↑+2H2O.
(4)C单质与Al具有某些相似性,比如能与强碱反应,写出C单质与NaOH溶液反应的化学方程式:Si+2NaOH+H2O═Na2SiO3+2H2↑.
(5)A、B、C、D均可形成分子中含18电子的氢化物,这些氢化物的分子式分别为H2S、C2H6、SiH4、N2H4.
| 元素 | A | B | C | D |
| 原子半径/nm | 0.102 | 0.077 | 0.117 | 0.075 |
| 最高正化合价 (或最低负化合价) | -4 | +4 |
(2)含D元素的两种常见共价化合物发生化合反应可生成一种离子化合物,该反应的化学方程式为NH3+HNO3═NH4NO3.
(3)B的单质与D的最高价氧化物对应的水化物在加热条件下发生反应的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$4NO2↑+CO2↑+2H2O.
(4)C单质与Al具有某些相似性,比如能与强碱反应,写出C单质与NaOH溶液反应的化学方程式:Si+2NaOH+H2O═Na2SiO3+2H2↑.
(5)A、B、C、D均可形成分子中含18电子的氢化物,这些氢化物的分子式分别为H2S、C2H6、SiH4、N2H4.
10.下列说法中正确的是( )
| A. | 将纯水加热至较高温度,Kw变大、pH变小、呈酸性 | |
| B. | 保存FeSO4溶液时,应在其中加入稀HNO3以抑制Fe2+水解 | |
| C. | 向0.1 mol•L-1 氨水中加入少量水,pH减小,$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$增大 | |
| D. | AlCl3溶液蒸干、灼烧至恒重,最终剩余固体是AlCl3 |
7.关于原电池的下列说法中,正确的是( )
| A. | 在负极上发生氧化反应 | B. | 化学性质较活泼的金属为负极 | ||
| C. | 在外电路上电子由负极流向正极 | D. | 是由电能转化为化学能的装置 |
14.下列反应中,属于氧化反应的是( )
| A. | 乙烷在光照下与氯气反应 | B. | 乙烯使酸性高锰酸钾溶液褪色 | ||
| C. | 乙烯使溴水褪色 | D. | 苯与液溴混合后撒入铁粉 |
11.下列有关氯气及其化合物的说法不正确的是( )
| A. | 因为氯气有毒,有强氧化性,所以可用于杀菌、消毒、漂白 | |
| B. | 干燥的氯气和氯水均能使鲜花褪色 | |
| C. | 除去氯气中少量氯化氢可使气体通过饱和食盐水 | |
| D. | 氯气能与大多数金属化合,其一般将变价金属氧化至最高价 |
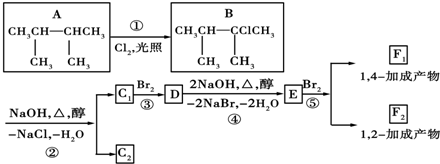
 .
. ;F1的结构简式是
;F1的结构简式是 .F1与F2的关系为同分异构体.
.F1与F2的关系为同分异构体.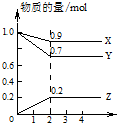 某温度时,在2L容器中X、Y、Z三种物质的量随时间的变化曲线如图所示.由图中数据分析.
某温度时,在2L容器中X、Y、Z三种物质的量随时间的变化曲线如图所示.由图中数据分析.