题目内容
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用.已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2O
Cd(OH)2+2Ni(OH)2有关该电池的说法正确的是( )
| 放电 |
| 充电 |
| A、充电时阳极反应:Ni(OH)2-e-+OH-=NiOOH+H2O |
| B、放电时负极附近溶液的pH不变 |
| C、放电时电解质溶液中的OH-向正极移动 |
| D、充电时Cd与外电源的正极相连 |
考点:化学电源新型电池
专题:
分析:该电池中,放电时,负极反应式为Cd-2e-+2OH-=Cd(OH)2,正极上发生的电极反应式为:NiOOH+e-+H2O═Ni(OH)2+OH-,充电时阳极上发生的电极反应式为:Ni(OH)2+OH--e-→NiOOH+H2O,阴极上发生的电极反应式为:Cd(OH)2+2e-═Cd+2OH-,放电时阴离子向负极移动、阳离子向正极移动,据此分析解答.
解答:
解:A.充电时,阳极上失电子发生氧化反应,电极反应式为Ni(OH)2-e-+OH-=NiOOH+H2O,故A正确;
B.放电时,负极反应式为Cd-2e-+2OH-=Cd(OH)2,氢氧根离子参加反应导致溶液碱性减弱,pH减小,故B错误;
C.放电时电解质溶液中的OH-向负极移动,故C错误;
D.充电时,Cd作阴极,则应该与外电源负极相连,故D错误;
故选A.
B.放电时,负极反应式为Cd-2e-+2OH-=Cd(OH)2,氢氧根离子参加反应导致溶液碱性减弱,pH减小,故B错误;
C.放电时电解质溶液中的OH-向负极移动,故C错误;
D.充电时,Cd作阴极,则应该与外电源负极相连,故D错误;
故选A.
点评:本题考查化学电源新型电池,明确各个电极上发生的反应是解本题关键,会正确书写电极反应式,知道离子移动方向,难点是电极反应式书写,要结合电解质溶液酸碱性书写,题目难度中等.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
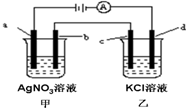 如图所示,a、b、c均为石墨电极,d为碳钢电极,通电进行电解.假设在电解过程中产生的气体全部逸出,下列说法正确的是( )
如图所示,a、b、c均为石墨电极,d为碳钢电极,通电进行电解.假设在电解过程中产生的气体全部逸出,下列说法正确的是( )| A、乙烧杯中的d电极反应式为Fe-2e-=Fe2+ |
| B、当电解一段时间后,将甲、乙两溶液混合,一定会沉淀 |
| C、当b极增重5.4g时,d极产生的气体为2.24L(标准状况) |
| D、甲烧杯中溶液的pH降低 |
下列物质与水反应,能放出氧气的是( )
| A、Na |
| B、Na2O |
| C、Na2O2 |
| D、NO2 |
对于密闭容器中进行的反应CO(g)+H2O(g)?CO2 (g)+H2(g),达到平衡后,其他条件不变,增大CO的浓度,下列说法不正确的是( )
| A、正反应速率增大 |
| B、逆反应速率先减小后增大 |
| C、达到平衡时,逆反应速率比原平衡要大 |
| D、CO的转化率降低 |
将SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个反应:SO2+2Fe3++2H2O═SO42-+4H++2Fe2+,Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O.下列说法正确的是( )
| A、氧化性:SO2可以被Cr2O72-氧化 |
| B、还原性:Cr3+>Fe2+>SO2 |
| C、Cr2O72-在反应中做还原剂 |
| D、两个反应中Fe3+均表现还原性 |
若某基态原子的外围电子排布为4d15s2,则下列说法不正确的是( )
| A、该元素位于第五周期IB族 |
| B、该元素原子核外有5个电子层 |
| C、该元素原子最外层共有2个电子 |
| D、该元素原子M层上共有18个电子 |