题目内容
“节能减排”,减少全球温室气体排放,意义十分重大.二氧化碳的捕捉与封存是实现温室气体减排的重要途径之一,科学家利用NaOH溶液喷淋“捕捉”空气中的CO2.
(1)使用过量NaOH溶液吸收CO2,反应的离子方程式为 ;若含有3molNaOH的溶液“捕捉”了22.4LCO2气体(标准状况),则所得溶液中钠与碳元素的物料守恒关系式为 (用离子浓度的关系式表示).
(2)①以CO2和NH3为原料可合成化肥尿素[CO(NH2)2].
已知:2NH3(g)+CO2(g)═NH2CO2NH4(s)△H=-159.47kJ?mol-1NH2CO2NH4(s)═CO(NH2)2(S)+H2O(g)△H=+72.49kJ?mol-1H2O(1)═H2O(g)△H=+44.0kJ?mol-1
试写出NH3和CO2合成尿素和液态水的热化学方程式 .
②CO2通过反应可转化为CO,在催化剂作用下CO和H2反应生成甲醇:CO(g)+2H2(g)?CH3OH(g),某容积可变的密闭容器中充有10molCO与20molH2,CO的平衡转化率(a)与温度、压强的关系如图所示.
a.若A点表示在某时刻达到的平衡状态,此时容器的容积为VL,则该温度下的平衡常数K= ;
平衡状态B点时容器的容积VB VL.(填“大于”、“小于”或“等于”)
b.若A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间tA tC(填“>”、“<”或“=”)
c.在不改变反应物用量的情况下,为提高CO的转化率可采取的措施是 (写出一种即可).

(1)使用过量NaOH溶液吸收CO2,反应的离子方程式为
(2)①以CO2和NH3为原料可合成化肥尿素[CO(NH2)2].
已知:2NH3(g)+CO2(g)═NH2CO2NH4(s)△H=-159.47kJ?mol-1NH2CO2NH4(s)═CO(NH2)2(S)+H2O(g)△H=+72.49kJ?mol-1H2O(1)═H2O(g)△H=+44.0kJ?mol-1
试写出NH3和CO2合成尿素和液态水的热化学方程式
②CO2通过反应可转化为CO,在催化剂作用下CO和H2反应生成甲醇:CO(g)+2H2(g)?CH3OH(g),某容积可变的密闭容器中充有10molCO与20molH2,CO的平衡转化率(a)与温度、压强的关系如图所示.
a.若A点表示在某时刻达到的平衡状态,此时容器的容积为VL,则该温度下的平衡常数K=
平衡状态B点时容器的容积VB
b.若A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间tA
c.在不改变反应物用量的情况下,为提高CO的转化率可采取的措施是
考点:转化率随温度、压强的变化曲线,热化学方程式,化学反应速率与化学平衡图象的综合应用
专题:基本概念与基本理论
分析:(1)使用过量NaOH溶液吸收CO2生成碳酸钠,根据元素守恒判断;
(2)①依据热化学方程式和盖斯定律计算①+②-③得到CO2与NH3合成尿素和液态水的热化学反应方程式.
②a.温度不变,平衡常数不变,根据A点温度下的转化率求平衡时各种物质的浓度,依据平衡常数概念计算得到;
B点转化率变大,平衡右移,体积变小;
b.温度越高,反应速率越快,达到平衡的时间越短;
c.提高CO的转化率可采取的措施是改变条件促使平衡正向进行.
(2)①依据热化学方程式和盖斯定律计算①+②-③得到CO2与NH3合成尿素和液态水的热化学反应方程式.
②a.温度不变,平衡常数不变,根据A点温度下的转化率求平衡时各种物质的浓度,依据平衡常数概念计算得到;
B点转化率变大,平衡右移,体积变小;
b.温度越高,反应速率越快,达到平衡的时间越短;
c.提高CO的转化率可采取的措施是改变条件促使平衡正向进行.
解答:
解:(1)使用过量NaOH溶液吸收CO2生成碳酸钠,反应离子方程式为CO2+OH-=CO32-+H2O;
22.4LCO2气体(标准状况)的物质的量为1mol,故Na和C元素的物质的量之比为3:1,C在溶液中以碳酸根离子、碳酸氢根离子和碳酸分子的形式存在,故钠与碳元素的物料守恒关系式为c(Na+)=3[c(CO32-)+c(HCO3-)+c(H2CO3)];
故答案为:CO2+OH-=CO32-+H2O;c(Na+)=3[c(CO32-)+c(HCO3-)+c(H2CO3)];
(2)①已知2NH3(g)+CO2(g)═NH2CO2NH4(s)△H=-159.47kJ?mol-1 ①
NH2CO2NH4(s)═CO(NH2)2(S)+H2O(g)△H=+72.49kJ?mol-1 ②
H2O(1)═H2O(g)△H=+44.0kJ?mol-1 ③
依据热化学方程式和盖斯定律计算①+②-③得到CO2与NH3合成尿素和液态水的热化学反应方程式为:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-130.98KJ/mol;
故答案为:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-130.98KJ/mol;
②a.CO(g)+2H2(g)?CH3OH(g)
初起浓度
mol/L
mol/L 0
变化浓度
mol/L
mol/L
mol/L
平衡浓度
mol/L
mol/L
mol/L
平衡常数K=
=0.01V2;
B点转化率变大,平衡右移,体积变小,VB小于VL;
故答案为:0.01V2;小于;
b.温度越高,反应速率越快,达到平衡的时间越短,C点温度高,达到平衡的时间短;故答案为:>;
c.反应是气体体积减小的放热反应,提高CO的转化率可采取的措施是降温、加压、分离出甲醇.故答案为:降温、加压、分离出甲醇.
22.4LCO2气体(标准状况)的物质的量为1mol,故Na和C元素的物质的量之比为3:1,C在溶液中以碳酸根离子、碳酸氢根离子和碳酸分子的形式存在,故钠与碳元素的物料守恒关系式为c(Na+)=3[c(CO32-)+c(HCO3-)+c(H2CO3)];
故答案为:CO2+OH-=CO32-+H2O;c(Na+)=3[c(CO32-)+c(HCO3-)+c(H2CO3)];
(2)①已知2NH3(g)+CO2(g)═NH2CO2NH4(s)△H=-159.47kJ?mol-1 ①
NH2CO2NH4(s)═CO(NH2)2(S)+H2O(g)△H=+72.49kJ?mol-1 ②
H2O(1)═H2O(g)△H=+44.0kJ?mol-1 ③
依据热化学方程式和盖斯定律计算①+②-③得到CO2与NH3合成尿素和液态水的热化学反应方程式为:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-130.98KJ/mol;
故答案为:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l)△H=-130.98KJ/mol;
②a.CO(g)+2H2(g)?CH3OH(g)
初起浓度
| 10 |
| V |
| 20 |
| V |
变化浓度
| 5 |
| V |
| 10 |
| V |
| 5 |
| V |
平衡浓度
| 5 |
| V |
| 10 |
| V |
| 5 |
| V |
平衡常数K=
| ||||
|
B点转化率变大,平衡右移,体积变小,VB小于VL;
故答案为:0.01V2;小于;
b.温度越高,反应速率越快,达到平衡的时间越短,C点温度高,达到平衡的时间短;故答案为:>;
c.反应是气体体积减小的放热反应,提高CO的转化率可采取的措施是降温、加压、分离出甲醇.故答案为:降温、加压、分离出甲醇.
点评:本题考查了热化学方程式和盖斯定律的计算应用,化学平衡标志判断,图象分析,影响平衡的因素分析判断,化学平衡移动原理是解题关键,题目难度中等.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
某化合物的结构(键线式)及球棍模型如图1:该有机分子的核磁共振氢谱图如图2(单位是ppm):下列关于该有机物的叙述正确的是( )
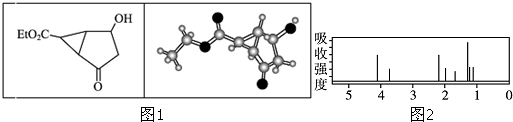

| A、该有机物不同化学环境的氢原子有6种 |
| B、该有机物属于芳香化合物 |
| C、键线式中的Et代表的基团为-CH3 |
| D、该有机物在一定条件下能够发生消去反应 |
下列叙述正确的是( )
| A、将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)=c(NH4+) |
| B、两种醋酸溶液的物质的量浓度分别c1和c2,pH分别为a和a+1,则c1<10c2 |
| C、室温下,pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,溶液呈酸性 |
D、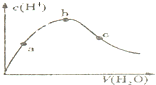 向冰醋酸中逐渐加水,有如图变化.a、b、c三点中水的电离程度最大的是b点 |
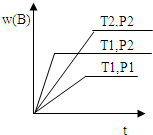 已知某反应aA(g)+bB(g)?cC(g)△H=Q 在密闭容器中进行,在不同温度(T1和T2 )及压强(P1 和P2 )下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示,下列判断正确的是( )
已知某反应aA(g)+bB(g)?cC(g)△H=Q 在密闭容器中进行,在不同温度(T1和T2 )及压强(P1 和P2 )下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示,下列判断正确的是( )| A、T1<T2,P1<P2,a+b>c,Q>0 |
| B、T1>T2,P1<P2,a+b<c,Q<0 |
| C、T1<T2,P1>P2,a+b<c,Q>0 |
| D、T1<T2,P1>P2,a+b>c,Q<0 |
在2SO2+O2=2SO3(正反应放热)的平衡体系中,下列条件可使反应速率加快,且平衡向右移动的是( )
| A、升高温度 |
| B、增加压强 |
| C、减小SO3的浓度 |
| D、使用催化剂 |
已知:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ?mol-1.现将一定量的稀盐酸、浓硫酸、稀醋酸分别和1L 1mol?L-1的NaOH溶液恰好完全反应,其反应热分别为△H1、△H2、△H3,则△H1、△H2和△H3的大小关系为( )
| A、△H1=△H2>△H3 |
| B、△H3>△H2>△H1 |
| C、△H2>△H1>△H3 |
| D、△H3>△H1>△H2 |
将质量分数为a%,物质的量浓度为c1 mol?L-1的稀H2SO4蒸发掉一定量的水,使之质量分数为2a%,此时物质的量浓度为c2 mol?L-1,则c1和c2的数值关系是( )
| A、c2=c1 |
| B、c2<2c1 |
| C、c2>2c1 |
| D、c2=2c1 |