题目内容
2.下列各对物质中属于同分异构体的是( )| A. | 16O和18O | B. | O2与O3 | C. | CH3CH2CH3与 | D. | 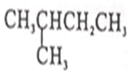 与 与 |
分析 同分异构体是分子式相同,结构不同的物质互为同分异构体.
解答 解:A.16O和18O的质子数相同,中子数不同的原子,互为同位素,故A错误;
B.O2和O3都是由氧元素组成的不同单质,互为同素异形体,故B错误;
C.CH3CH2CH3与 都是烷烃,结构相似,在分子组成上相差1个CH2,互为同系物,故C错误;
都是烷烃,结构相似,在分子组成上相差1个CH2,互为同系物,故C错误;
D.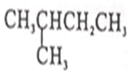 与
与 的分子式相同,结构不同,互为同分异构体,故D正确.
的分子式相同,结构不同,互为同分异构体,故D正确.
故选D.
点评 本题主要考查了同分异构体的概念,难度不大,明确同分异构体中:“同”为分子式相同,“异”为结构相异是解本题的关键.

练习册系列答案
相关题目
6.湿润的淀粉碘化钾试纸接触某气体而显蓝色,该气体可能是( )
①氯气;②碘蒸气;③溴化钾;④溴化氢;⑤氯化氢;⑥溴蒸气.
①氯气;②碘蒸气;③溴化钾;④溴化氢;⑤氯化氢;⑥溴蒸气.
| A. | ①③④ | B. | ①②⑤ | C. | ①②⑥ | D. | ②④⑤ |
13.如图选用的相关仪器(固定装置略去)符合实验要求的是( )
| A. |  存放浓硝酸 | B. | 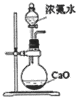 可用于制备氨气 | ||
| C. | 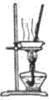 蒸干氯化铝溶液AlCl3•6H2O晶体 | D. |  实验室抽取乙烯 |
10.将标准状况下的V L HCl(气)溶于1 000g水中,得到的盐酸密度为ρ g•cm-3,则该盐酸的物质的量浓度为( )
| A. | $\frac{1000Vρ}{22400+36.5V}$ mol•L-1 | B. | $\frac{Vρ}{22400}$ mol•L-1 | ||
| C. | $\frac{Vρ}{22400+36.5V}$ mol•L-1 | D. | $\frac{V}{22.4}$ mol•L-1 |
7.下列判断不正确的是( )
| A. | 碱性氧化物一定是金属氧化物 | |
| B. | 有元素化合价升降的反应一定是氧化还原反应 | |
| C. | 在D216O中,质量数之和是质子数之和的两倍 | |
| D. | 通式相同,相差一个或若干个“CH2”原子团的有机物一定为同系物 |
14.下列过程中,发生氧化还原反应的是( )
| A. | Cu和稀HNO3反应 | B. | Fe导电 | ||
| C. | Na2CO3溶液与盐酸反应 | D. | 实验室制取NH3 |
11.用固体氢氧化钠配制一定物质的量浓度溶液时,下列说法正确的是( )
| A. | 称量固体氢氧化钠时托盘天平两边放大小一样的白纸 | |
| B. | 配置溶液时洗涤烧杯和玻璃棒,引起所得溶液浓度偏高 | |
| C. | 容量瓶使用前未经干燥会导致所得溶液浓度偏低 | |
| D. | 容量瓶、分液漏斗、滴定管使用前都要检查是否漏水 |
12.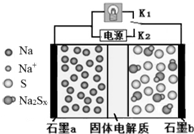 高温钠硫电池是一种新型可充电电池,其工作原理如图所示,图中固体电解质是Na+导体.下列叙述正确的是( )
高温钠硫电池是一种新型可充电电池,其工作原理如图所示,图中固体电解质是Na+导体.下列叙述正确的是( )
 高温钠硫电池是一种新型可充电电池,其工作原理如图所示,图中固体电解质是Na+导体.下列叙述正确的是( )
高温钠硫电池是一种新型可充电电池,其工作原理如图所示,图中固体电解质是Na+导体.下列叙述正确的是( )| A. | 放电时,石墨电极a为正极 | |
| B. | 放电时,Na+从石墨b向石墨a方向迁移 | |
| C. | 可将装置中的固体电解质改成NaCl溶液 | |
| D. | 充电时,b极反应为Na2Sx-2e-=xS+2Na+ |
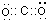 ;一种由B、C组成的化合物与AC2互为等电子体,其分子式为N2O,其结构式为O=N=N.
;一种由B、C组成的化合物与AC2互为等电子体,其分子式为N2O,其结构式为O=N=N. ,E的基态原子的简化电子排布式是[Ar]3d54s1.ECl3形成的配合物的化学式为[Cr(NH3)4(H2O)2]Cl3.
,E的基态原子的简化电子排布式是[Ar]3d54s1.ECl3形成的配合物的化学式为[Cr(NH3)4(H2O)2]Cl3.