题目内容
摩尔质量的符号为 单位是 ;CO2的摩尔质量为 ,88g CO2的物质的量为 ,所含二氧化碳分子数为 (用NA表示阿伏加德罗常数,下同),含有 个氧原子,与 g H2O气体所含氧原子数相同;0.01mol某气体的质量为0.28g,该气体的相对分子质量为 ;已知3.01×1023个某分子A的质量为8g,则A的摩尔质量为 .
考点:物质的量的相关计算
专题:计算题
分析:摩尔质量符号为M,常用单位为g/mol,数值上等于物质的相对分子质量,根据n=
计算88g CO2的物质的量,根据N=nNA计算CO2的分子数目,氧原子数目为二氧化碳分子的2倍;水与二氧化碳含有相同氧原子数目,则水的物质的量为二氧化碳的2倍,根据m=nM计算水的质量;根据m=
计算该气体摩尔质量,进而确定该气体相对分子质量;根据n=
计算分子A的物质的量,根据m=
计算A的摩尔质量.
| m |
| M |
| m |
| n |
| N |
| NA |
| m |
| n |
解答:
解:摩尔质量符号为M,常用单位为g/mol,CO2的摩尔质量为44g/mol,88g CO2的物质的量为
=2mol,根据N=nNA计算CO2的分子数目=2mol×mol-1=2NA,氧原子数目为二氧化碳分子的2倍,含有氧原子数目为4NA;水与二氧化碳含有相同氧原子数目,则水的物质的量为二氧化碳的2倍,故水的质量为4mol×18g/mol=72g;
该气体摩尔质量为
=28g/mol,故该气体相对分子质量为28;
分子A的物质的量为
=0.5mol,A的摩尔质量为
=16g/mol,
故答案为:M;g/mol;44g/mol;2NA;4NA;72;28;16g/mol.
| 88g |
| 44g/mol |
该气体摩尔质量为
| 0.28g |
| 0.01mol |
分子A的物质的量为
| 3.01×1023 |
| 6.02×1023mol-1 |
| 8g |
| 0.5mol |
故答案为:M;g/mol;44g/mol;2NA;4NA;72;28;16g/mol.
点评:本题考查摩尔质量、物质的量有关计算,比较基础,侧重对基础知识的巩固.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
通常所说的“白色污染”指的是( )
| A、白色建筑废料 |
| B、石灰窑的白色粉尘 |
| C、冶炼厂的白色烟尘 |
| D、聚乙烯等塑料垃圾 |
如图是X、Y两种固体物质的溶解度曲线,下列说法不正确的是( )
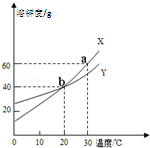

| A、将20℃的饱和溶液X降温到10℃,溶液X仍然是饱和溶液 |
| B、a点表示30℃时,X的溶解度为60g |
| C、b点表示20℃时,X、Y的溶解度相等 |
| D、同质量的X、Y饱和溶液分别从30℃降到10℃时,析出的Y的质量大于X的质量 |
常温下c(H+)最小的是( )
| A、pH=0的溶液. |
| B、0.03 mol?L-1 H2SO4. |
| C、0.05 mol?L-1 HClO |
| D、0.05 mol?L-1的NaHSO4. |
设NA表示阿伏加德罗常数,下列叙述中不正确的是( )
| A、31g仅含有少量白磷,无其他杂质的红磷样品中,共含有NA个磷原子 |
| B、假设1mol氯化铁完全转化为氢氧化铁胶体,则分散系中胶体微粒数小于NA |
| C、1molNa2O2与水反应转移的电子数为NA |
| D、58.5g的氯化钠固体中含有NA个氯化钠分子 |
下列离子方程式正确的是( )
| A、澄清的石灰水与盐酸反应 Ca(OH)2+2H+═Ca2++2H2 O |
| B、钠与水的反应 Na+2H2 O═Na++2OH-+H2↑ |
| C、铜片插入硝酸银溶液 Cu+Ag+═Cu2++Ag |
| D、大理石溶于醋酸 CaCO3+2CH3COOH═Ca2++2CH3COO-+H2O+CO2↑ |
已知:①2C(s)+O2(g)═2CO(g)△H=-221.0kJ?mol-1;
②2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1.
则制备水煤气的反应C(s)+H2O(g)═CO(g)+H2(g)的△H为( )
②2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1.
则制备水煤气的反应C(s)+H2O(g)═CO(g)+H2(g)的△H为( )
| A、262.6 kJ?mol-1 |
| B、-131.3 kJ?mol-1 |
| C、-352.3 kJ?mol-1 |
| D、131.3 kJ?mol-1 |
