题目内容
16.取三个干燥的烧瓶,分别装入标准状况下的干燥氨气、含有二分之一体积空气的氯化氢、二氧化氮和氧气(体积比为4:1)的混合气体;然后分别做溶解于水的喷泉实验.实验结束后三个烧瓶中所得溶液的物质的量浓度之比为( )| A. | 2:1:2 | B. | 5:5:4 | C. | 1:1:1 | D. | 无法确定 |
分析 干燥纯净的氨气,含一半空气的氯化氢气体,这两个是一样的,他们都是$\frac{1}{22.4}$mol/L,因为每当溶解1L气体时会进入溶液是1L,此时溶质的物质的量是$\frac{1}{22.4}$mol/L,二氧化氮和氧气(体积比为4:1)的烧瓶根据反应4NO2+O2+2H2O=4HNO3来进行计算.
解答 解:假设烧瓶体积为5V,则干燥纯净的氨气体积为5V完全溶于水后烧瓶充满溶液溶液体积也是5V,溶质物质的量浓度为:$\frac{\frac{5V}{22.4}}{5V}$=$\frac{1}{22.4}$(mol/L);
含一半空气的氯化氢烧瓶中氯化氢体积为2.5V完全溶解后烧瓶进水$\frac{1}{2}$,也就是溶液体积为2.5V,所以溶质物质的量浓度为:$\frac{\frac{2.5V}{22.4}}{2.5V}$=$\frac{1}{22.4}$(mol/L);
二氧化氮与氧气体积比为$\frac{4}{1}$的混合气中NO2体积为4V,
根据以下方程式恰好完全反应:4NO2+O2+2H2O=4HNO3,而且生成硝酸物质的量为$\frac{4V}{22.4}$(mol),
由于完全反应所以烧瓶充满溶液其体积为5V,所以溶质的物质的量浓度为:$\frac{\frac{4V}{22.4}}{5V}$=$\frac{0.8V}{22.4}$(mol/L).
所以三个烧瓶中所得溶液的溶质的物质的量浓度之比为:$\frac{1}{22.4}$(mol/L):$\frac{1}{22.4}$(mol/L):$\frac{0.8V}{22.4}$(mol/L)=1:1:0.8=5:5:4,
故选B.
点评 本题考查物质的量浓度的计算,题目难度中等,明确二氧化氮与水的反应原理为解答关键,根据物质的量浓度的计算公式进行计算,试题培养了学生的化学计算能力.


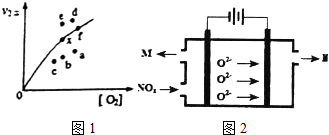
| A. | 该过程是化学能转化为电能的过程 | |
| B. | 一段时间后,①池中n(KHCO3)不变 | |
| C. | 一段时间后,②池中溶液的pH一定增大 | |
| D. | 铜电极的电极反应式为:CO2+6H2O+8e-═CH4+8 OH- |
| A. | 原子半径:A<B | B. | 原子序数:A>B | ||
| C. | 原子最外层上电子数:A>B | D. | A的正价与B的负价的绝对值相等 |
| A. | 0.1mol•L-1稀硫酸中含有硫酸根个数为0.1NA | |
| B. | 7.8g过氧化钠与足量水充分反应转移电子0.1NA | |
| C. | 2.4g金属镁与足量的盐酸反应,生成氢气的体积为2.24L | |
| D. | 标准状况下,0.5NA个水分子所占体积是11.2L |
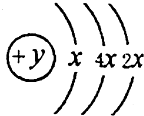 A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图如图,B、C可形成离子化合物B2C或B2C2,据此填空:
A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图如图,B、C可形成离子化合物B2C或B2C2,据此填空: