题目内容
下列说法中不正确的是( )
| A、电负性的大小顺序为Cl>S>P |
| B、由于NO3-和SO3互为等电子体,所以可以推断NO3-的空间构型为平面三角形 |
| C、根据晶格能的大小可以判断MgCl2的熔点比CaCl2高 |
| D、液态HF的沸点比液态HCl的沸点高是因为氢氟键的键能比氢氯键的键能大. |
考点:判断简单分子或离子的构型,元素电离能、电负性的含义及应用,晶格能的应用,氢键的存在对物质性质的影响
专题:化学键与晶体结构
分析:A.同一周期元素,元素的电负性随着原子序数的增大而增大;
B.等电子体原子个数相等、价电子数相等,且结构相似;
C.离子晶体中,晶格能大小与离子半径成反比、与电荷成正比;
D.氢键的存在导致物质的沸点升高.
B.等电子体原子个数相等、价电子数相等,且结构相似;
C.离子晶体中,晶格能大小与离子半径成反比、与电荷成正比;
D.氢键的存在导致物质的沸点升高.
解答:
解:A.同一周期元素,元素的电负性随着原子序数的增大而增大,这三种元素的电负性大小顺序是Cl>S>P,故A正确;
B.等电子体原子个数相等、价电子数相等,且结构相似,NO3-和SO3互为等电子体,NO3-的价层电子对个数=3+
×(5+1-3×2)=3,则该微粒是平面三角形结构,故B正确;
C.离子晶体中,晶格能大小与离子半径成反比、与电荷成正比,氯化镁和氯化钙中阴离子相同,阳离子不同,镁离子半径小于钙离子,所以氯化镁的晶格能大于氯化钙,则氯化镁的熔点高于氯化钙,故C正确;
D.HF中存在氢键、HCl中不存在氢键,氢键的存在导致HF的沸点高于HCl,故D错误;
故选D.
B.等电子体原子个数相等、价电子数相等,且结构相似,NO3-和SO3互为等电子体,NO3-的价层电子对个数=3+
| 1 |
| 2 |
C.离子晶体中,晶格能大小与离子半径成反比、与电荷成正比,氯化镁和氯化钙中阴离子相同,阳离子不同,镁离子半径小于钙离子,所以氯化镁的晶格能大于氯化钙,则氯化镁的熔点高于氯化钙,故C正确;
D.HF中存在氢键、HCl中不存在氢键,氢键的存在导致HF的沸点高于HCl,故D错误;
故选D.
点评:本题考查较综合,涉及氢键、等电子体、晶格能、电负性等知识点,根据元素周期律、等电子体特点、晶格能的影响因素等知识点来分析解答,会利用价层电子对互斥理论确定微粒构型,为学习难点.

练习册系列答案
相关题目
欲增大铁与酸反应放出氢气的速率,下列措施中不正确的是( )
| A、用铁粉代替铁片 |
| B、提高反应温度 |
| C、用浓硫酸代替稀硫酸 |
| D、去除铁表面的铁锈 |
某中药的有效成分M具有清炎杀菌作用,M的结构如图所示 :已知
:已知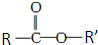 和NaOH反应能生成RCOONa和R′OH,下列叙述正确的是( )
和NaOH反应能生成RCOONa和R′OH,下列叙述正确的是( )
 :已知
:已知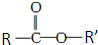 和NaOH反应能生成RCOONa和R′OH,下列叙述正确的是( )
和NaOH反应能生成RCOONa和R′OH,下列叙述正确的是( )| A、M的相对分子质量是180 |
| B、1mol M最多能与2mol Br2发生反应 |
| C、M与足量的Na溶液发生反应时,所得有机产物的化学式为C9H4O4Na2 |
| D、1mol M与足量NaHCO3反应能生成2mol CO2 |
一元酯A在酸性条件下水解得到一元饱和羧酸M与醇N(分子式为C5H12O),且醇N在一定条件下可氧化为M.则此酯A最多有几种结构( )
| A、4种 | B、3种 |
| C、16种 | D、32种 |
在恒温下容积固定的密闭容器中,能充分说明反应 2NO+O2?2NO2 已达到平衡状态的是( )
| A、反应容器中的气体压强不随时间而变化 |
| B、生成O2的速率与生成NO2的速率相等 |
| C、NO、O2、NO2各浓度之比为2:1:2 |
| D、混合气体的密度一定 |
从理论上分析,碳原子数小于10的烷烃分子中,其一卤代物不存在同分异构体的烷烃分子共有的种数是( )
| A、3 | B、4 | C、5 | D、6 |
下列离子方程式正确的是( )
| A、Fe3O4与稀硝酸反应:Fe3O4+8H+=Fe2++2Fe3++4H2O |
| B、SO2通入Ba(NO3)2溶液中:Ba2++SO2+H2O=BaSO3↓+2H+ |
| C、硫酸铵溶液与Ba(OH)2溶液反应:Ba2++SO42-=BaSO4↓ |
| D、FeBr2溶液与等物质的量的Cl2反应:2Fe2++2Br-+2Cl2=2Fe3++4Cl-+Br2 |
下列溶液中,阴离子浓度最大的是( )
| A、0.5mol/L HCl溶液50mL |
| B、0.6mol/L Al2(SO4)3溶液40mL |
| C、0.7mol/L NaCl溶液70mL |
| D、0.8mol/L Na2CO3溶液60mL |
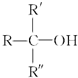 不能被氧化剂氧化(R,R′,R″均表示烃基),根据上述反应机理回答下列问题:
不能被氧化剂氧化(R,R′,R″均表示烃基),根据上述反应机理回答下列问题: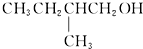 在有Cu和加热条件下与O2反应的化学方程式
在有Cu和加热条件下与O2反应的化学方程式