题目内容
5.用NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 由2H和18O所组成的水11 g,所含的中子数为4NA | |
| B. | 1 mol N2与4 mol H2反应生成的NH3分子数为2NA | |
| C. | 标准状况下,7.1 g氯气与足量石灰乳充分反应转移电子数为0.2NA | |
| D. | NO2和H2O反应每生成2 mol HNO3时转移的电子数目为2NA |
分析 A、求出11g2H218O的物质的量,然后根据1mol2H218O中含12mol中子来分析;
B、合成氨的反应为可逆反应;
C、求出氯气的物质的量,然后根据氯气和碱的反应为歧化反应来分析;
D、二氧化氮和水反应时,3molNO2反应转移2mol电子.
解答 解:A、11g2H218O的物质的量为0.5mol,而1mol2H218O中含12mol中子,故0.5mol2H218O中含6NA个中子,故A错误;
B、合成氨的反应为可逆反应,故不能进行彻底,故生成的氨气分子个数小于2NA个,故B错误;
C、7.1g氯气的物质的量为0.1mol,而氯气和碱的反应为歧化反应,故0.1mol氯气转移0.1NA个电子,故C错误;
D、二氧化氮和水反应时,3molNO2反应转移2mol电子,生成2mol硝酸,故当生成2mol硝酸时,转移2NA个电子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
相关题目
15.下列离子方程式正确的是( )
| A. | NaHCO3溶液和过量NaOH溶液混合HCO3-+OH-=CO32-+H2O | |
| B. | 在氢氧化钠溶液中滴加少量氯化铝 Al3++3OH-=Al(OH)3↓ | |
| C. | 将少量稀盐酸滴加到碳酸钠溶液中:2H++CO32-=H2O+CO2↑ | |
| D. | 向硫酸铝钾溶液中滴加氢氧化钡溶液至沉淀物质的量最多3Ba2++6OH-+2Al3++3SO42-═3BaSO4↓+2Al(OH)3↓ |
10.某饱和溶液中含有三种阳离子:Cu2+、Ba2+、Al3+,同时测知此溶液中pH=3,则该溶液所含有的阴离子可以是下列中的( )
| A. | CO32- | B. | SO42- | C. | Cl- | D. | S2- |
14.下列物质中,有1种与另外3种颜色不同,该物质是( )
| A. | 氢氧化钠 | B. | 碳酸钠 | C. | 氧化钠 | D. | 过氧化钠 |


 .
. .
.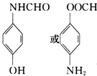 .
. 的合成路线补充完整.
的合成路线补充完整.
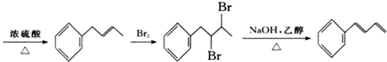 (无机试剂及溶剂任选).
(无机试剂及溶剂任选). ,X2Y
,X2Y