题目内容
某溶液中大量存在如下五种离子:NO3-、SO42-、Fe3+、H+、M,它们的物质的量之比依次为n(NO3-):n(SO42-):n(Fe3+):n(H+):n(M)=2:3:1:3:1,则M可能是( )
| A、Al3+ |
| B、Mg2+ |
| C、CO32- |
| D、Ba2+ |
考点:离子共存问题
专题:离子反应专题
分析:结合电荷守恒判断M离子的电荷,根据离子之间不能结合生成沉淀、气体、水等,则离子大量共存,以此来解答.
解答:
解:n(NO3-):n(SO42-):n(Fe3+):n(H+):n(M)=2:3:1:3:1,
由电荷守恒可知,2×1+3×2<1×3+3×1,
则M为阳离子,设M中离子电荷数为x,则2×1+3×2=1×3+3×1+1×x,
x=2,
B、D均符合,但Ba2+、SO42-结合生成沉淀,不能大量共存,
故选B.
由电荷守恒可知,2×1+3×2<1×3+3×1,
则M为阳离子,设M中离子电荷数为x,则2×1+3×2=1×3+3×1+1×x,
x=2,
B、D均符合,但Ba2+、SO42-结合生成沉淀,不能大量共存,
故选B.
点评:本题考查离子的共存,为高频考点,把握离子之间的反应及电荷守恒为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
雅琴的班主任王老师最近带了一副变色眼镜,有关这些玻璃知识说法正确的是( )
| A、钢化玻璃不是玻璃 |
| B、普通玻璃加入氧化钴会呈现红色 |
| C、加入氧化铅后制得的光学玻璃折光率高 |
| D、钢化玻璃比普通玻璃机械强度小 |
关于氯气的叙述中,下列说法正确的是( )
| A、氯气是一种黄绿色、有毒的气体 |
| B、氯气可以与铁反应生成FeCl2 |
| C、氯气不能溶于水,所以可用排水法收集氯气 |
| D、氯气、氯水、液氯是同一种物质,只是状态不同,都属于纯净物 |
下列说法不正确的是( )
| A、非金属气态氧化物都不是电解质 |
| B、SO2、NO2、C02都会导致酸雨的形成 |
| C、氮的氧化物都属于大气污染物 |
| D、Si、S的氧化物均属于酸性氧化物 |
下列热化学方程式中△H的绝对值能表示可燃物的燃烧热的是( )
A、
| ||||
| B、CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-802.3kJ/mol | ||||
| C、2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/mol | ||||
D、CO(g)+
|
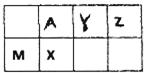 五种短周期元素在周期表中的位置如图,其中M、X、Z在地壳中的含量居前三位.
五种短周期元素在周期表中的位置如图,其中M、X、Z在地壳中的含量居前三位.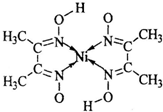 太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层.
太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层.