题目内容
3.已知:氟硼酸(HBF4)是强酸,Pb(BF4)2是可溶于水的强电解质,某二次电池能在低温下工作,其工作原理是Pb+PbO2+4HBF4$?_{充电}^{放电}$2Pb(BF4)2+2H2O,下列说法正确的是( )| A. | 放电时,正极区的pH增大 | |
| B. | 放电时,负极的电极反应式为PbO4+4H++2e-═Pb2++2H2O | |
| C. | 充电时,铅电极与电源的正极相连 | |
| D. | 充电时,当阴极生成20.7g Pb时溶液中有0.2mol电子通过 |
分析 A、放电时正极上发生还原反应,根据电极反应式来判断;
B、放电时,负极上发生失电子的氧化反应;
C、电池在充电时,负极和电源的负极相连,正极和正极相连;
D、20.7g Pb的物质的量为0.1mol,而生成1molPb转移2mol的电子.
解答 解:A、放电时正极上发生还原反应,PbO2+4H++2e-═Pb2++2H2O,氢离子浓度减小,所以pH增大,故A正确;
B、放电时,负极上应该是金属铅发生失电子的氧化反应,不是还原反应,故B错误;
C、充电时,Pb电极和电源的负极相连,故C错误;
D、20.7g Pb的物质的量为0.1mol,而生成1molPb转移2mol的电子,所以充电时,当阴极生成20.7g Pb时溶液中有0.2mol电子通过,故D正确;
故选AD.
点评 本题考查了电化学的相关知识,根据元素化合价变化确定电极,再结合电极反应式来分析解答,难度中等.

练习册系列答案
相关题目
13.下列各组物质含有的化学键类型完全相同的是( )
| A. | HBr、CO2、NH3 | B. | Na2O、Na2O2、Na2S | C. | NaCl、HCl、H2O | D. | NaOH、CaCl2 |
14.常温时,用0.1000mol/L NaOH溶液滴定25.00mL 0.1000mol/L某一元酸HX溶液,滴定过程中pH变化曲线如图所示.下列说法不正确的是( )
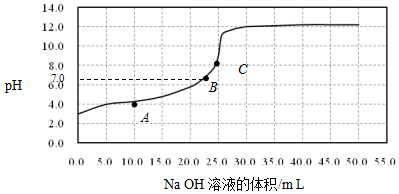

| A. | 在A点:c(HX)>c(Na+)>c(X-) | |
| B. | 在B点,溶液中c(H+)=c(OH-) | |
| C. | C点溶液中存在的主要平衡是X-+H2O?HX+OH- | |
| D. | 0.05mol/L NaX溶液的pH≈9 |
8.锌和锌的化合物用途广泛,可用于作防腐镀层、电池、白色颜料和防晒剂等,查阅资料可知:1mol H2O(g)完全凝结为液态,放出44.0kJ热量
(1)利用锌和太阳能分解水循坏制氢的示意图如下.“装置A”指虚线框中体系,太阳炉能聚焦太阳能而产生高温.
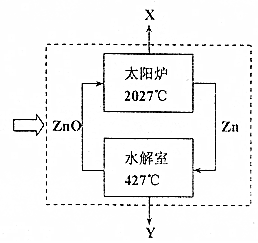
①下列有关叙述中不正确的是a
a.装置A只将太阳能转化为化学能
b.太阳炉中须首要解决的问题是产物的及时分离和冷却
c.该法与电解水制氢相比的优点:H2与O2分步产生,不须考虑隔离问题
②生产过程中不断向装置A中输入太阳光和水;装置A可向外输出的物质X、Y分别为氧气、氢气;整个生产过程中循环利用的物质为锌
③H2的燃烧热为285.5KJ/mol,1molZnO完全分解生成液态锌和氧气时吸收350.5kJ热量,写出水解室中反应的热化学方程式(假设维持常压)Zn(S)+H2O(g)=ZnO (S)+H2(g)△H=-109KJ/mol
(2)闪锌矿(ZnS)是锌的主要矿物之一,是提取锌的重要原料,纯净的ZnS可作白色颜料
①计算反应ZnS+Cu2+?Zn2++CuS在常温下的平衡常数K=3.91×1013
②下列叙述不正确的是C
a.常温下,CuS不能溶于稀硫酸
b.常温下,ZnS与0.2mol/LCuSO4溶液作用,固体由白变黑
c.常温下,向饱和CuSO4溶液中通入H2S,无明显现象
d.常温下,0.1molBaS(易溶)可使100mL1mol/ZnSO4溶液的离子沉淀完全
③火法炼锌是在空气中煅烧ZnS首先得到ZnO,再用炭等热还原出锌,而湿法炼锌是先将ZnO转为为ZnSO4,再以铝和石墨分别为两电极电解ZnSO4溶液,金属锌便以99.95%的纯度沉积在铝电极上,电解时的阳极反应为4OH--4e-=2H2O+O2↑.
| Zn | ZnO | ZnS | CuS | BaSO4 | H2S | |
| 熔点/℃ | 419.5 | 1975(同时分解) | - | - | - | - |
| 沸点/℃ | 907 | - | - | - | - | - |
| Ksp(常温) | - | - | 2.5×10-21 | 6.4×10-35 | 1.1×10-10 | K1=1.1×10-7 K2=1.3×10-13 |

①下列有关叙述中不正确的是a
a.装置A只将太阳能转化为化学能
b.太阳炉中须首要解决的问题是产物的及时分离和冷却
c.该法与电解水制氢相比的优点:H2与O2分步产生,不须考虑隔离问题
②生产过程中不断向装置A中输入太阳光和水;装置A可向外输出的物质X、Y分别为氧气、氢气;整个生产过程中循环利用的物质为锌
③H2的燃烧热为285.5KJ/mol,1molZnO完全分解生成液态锌和氧气时吸收350.5kJ热量,写出水解室中反应的热化学方程式(假设维持常压)Zn(S)+H2O(g)=ZnO (S)+H2(g)△H=-109KJ/mol
(2)闪锌矿(ZnS)是锌的主要矿物之一,是提取锌的重要原料,纯净的ZnS可作白色颜料
①计算反应ZnS+Cu2+?Zn2++CuS在常温下的平衡常数K=3.91×1013
②下列叙述不正确的是C
a.常温下,CuS不能溶于稀硫酸
b.常温下,ZnS与0.2mol/LCuSO4溶液作用,固体由白变黑
c.常温下,向饱和CuSO4溶液中通入H2S,无明显现象
d.常温下,0.1molBaS(易溶)可使100mL1mol/ZnSO4溶液的离子沉淀完全
③火法炼锌是在空气中煅烧ZnS首先得到ZnO,再用炭等热还原出锌,而湿法炼锌是先将ZnO转为为ZnSO4,再以铝和石墨分别为两电极电解ZnSO4溶液,金属锌便以99.95%的纯度沉积在铝电极上,电解时的阳极反应为4OH--4e-=2H2O+O2↑.
15.兵马俑中所用颜料成分一直是个谜,近年来科学家才得知大多为硅酸盐,如蓝紫色的硅酸铜钡(BaCuSi2Ox,铜为+2价),下列关于硅酸铜钡的说法错误的是( )
| A. | x等于6 | |
| B. | 性质稳定,不易脱色 | |
| C. | 易溶解于强酸和强碱 | |
| D. | 可用氧化物形式表示为BaO•CuO•2SiO2 |
12.用NA表示阿伏伽德罗常数的值,下列说法中正确的是( )
| A. | 1 mol/L CaCl2溶液中含有Cl-的数目为NA | |
| B. | 标准状况下,2.24L HF所含分子数一定为0.1NA | |
| C. | 6.4g S6与S8的混合物中所含S原子数一定为0.2NA | |
| D. | 标准状况下,2.24L 氧元素的单质所含原子数一定为0.2NA |
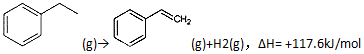
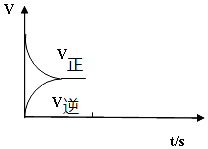
 (1)常温下,0.5mol甲醇在氧气中充全燃烧生成CO2和液态水,放出热量363.3kJ.写 出甲醇燃烧的热化学方程式CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-726.6kJ•mol-1.
(1)常温下,0.5mol甲醇在氧气中充全燃烧生成CO2和液态水,放出热量363.3kJ.写 出甲醇燃烧的热化学方程式CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-726.6kJ•mol-1.