题目内容
下列有关物质的性质与其应用不相对应的是( )
| A、Al具有良好的延展性和抗腐蚀性,可制成铝箔包装物品 |
| B、NaHCO3能与碱反应,食品工业用作焙制糕点的膨松剂 |
| C、晶体硅是半导体材料,可用于计算机芯片的基底 |
| D、K2FeO4能与水作用生成Fe(OH)3胶体和O2,可用于自来水的净化和杀菌消毒 |
考点:钠的重要化合物,硅和二氧化硅,铝的化学性质
专题:碳族元素,几种重要的金属及其化合物
分析:A、铝能制成铝箔是因为铝具有良好的延展性和防腐性;
B、食品工业用作焙制糕点的膨松剂,利用碳酸氢钠和酸反应生成二氧化碳气体;
C、硅可用于制造半导体材料,高纯度的晶体硅被广泛用于制作计算机芯片;
D、氢氧化铁胶体具有吸附作用吸附悬浮杂质,K2FeO4是强氧化剂杀菌消毒.
B、食品工业用作焙制糕点的膨松剂,利用碳酸氢钠和酸反应生成二氧化碳气体;
C、硅可用于制造半导体材料,高纯度的晶体硅被广泛用于制作计算机芯片;
D、氢氧化铁胶体具有吸附作用吸附悬浮杂质,K2FeO4是强氧化剂杀菌消毒.
解答:
解:A、铝能制成铝箔是因为铝具有良好的延展性和防腐性,铝表面氧化铝性质稳定,可制成铝箔包装物品,故A正确;
B、食品工业用作焙制糕点的膨松剂,利用碳酸氢钠和酸反应生成二氧化碳气体,不是利用NaHCO3能与碱反应的性质,故B错误;
C、因为硅是半导体材料,所以高纯度的晶体硅被广泛用于制作计算机芯片,故C正确;
D、氢氧化铁胶体具有吸附作用吸附悬浮杂质,K2FeO4是强氧化剂杀菌消毒,可用于自来水的净化和杀菌消毒,故D正确;
故选B.
B、食品工业用作焙制糕点的膨松剂,利用碳酸氢钠和酸反应生成二氧化碳气体,不是利用NaHCO3能与碱反应的性质,故B错误;
C、因为硅是半导体材料,所以高纯度的晶体硅被广泛用于制作计算机芯片,故C正确;
D、氢氧化铁胶体具有吸附作用吸附悬浮杂质,K2FeO4是强氧化剂杀菌消毒,可用于自来水的净化和杀菌消毒,故D正确;
故选B.
点评:本题考查了铝、碳酸氢钠、硅、氢氧化铁等物质性质的应用和用途,掌握物质性质,熟悉物质用途的依据是解题关键,题目难度中等.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
下列物质的鉴别方法不正确的是( )
| A、利用丁达尔效应鉴别Fe(OH)3胶体与FeCl3溶液 |
| B、用氢氧化钠溶液鉴别MgCl2溶液、AlCl3溶液 |
| C、用焰色反应鉴别NaCl、KCl和Na2SO4 |
| D、用氯化钙溶液鉴别Na2CO3和NaHCO3两种溶液 |
根据表中提供的数据判断下列说法不正确的是( )
| 化学式 | 电离常数(25℃) |
| HCN | K=5.0×10-10 |
| H2CO3 | K1=4.3×10-7 |
| K2=5.6×10-11 |
| A、等浓度等体积的NaCN、NaHCO3溶液混合:c(Na+)+c(H+)=c(HCO3-)+c(CN-)+c(OH-)+2c(CO32-) | ||
B、若NaCN的水解平衡常数为:Kh=
| ||
| C、等浓度等体积的NaCN和NaCl溶液中离子数目前者大于后者 | ||
| D、过量CO2通入NaCN溶液中:CO2+H2O+CN-=HCO3-+HCN |
下列叙述正确的是( )
| A、漂白粉的有效成分是Ca(ClO)2 |
| B、浓硝酸在光照下颜色变黄,说明浓硝酸易挥发 |
| C、绿色食品是不含任何化学物质的食品 |
| D、在空气质量日报中CO2属于污染物. |
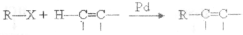
 ),在一定条件下能发生银镜反应,且1molE最多可得到4molAg;
),在一定条件下能发生银镜反应,且1molE最多可得到4molAg;
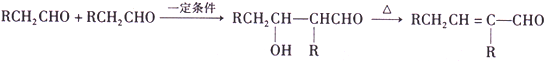
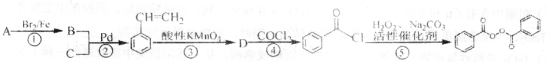
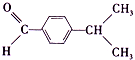 )合成兔耳草醛的路线如下:
)合成兔耳草醛的路线如下: