题目内容
下列说法正确的是 ( )
A.H2O的熔点、沸点大于H2S的是由于H2O分子之间存在氢键。
B.HF、HCl、HBr、HI的熔点沸点依次升高。
C.乙醇分子与水分子之间只存在范德华力。
D.氯的各种含氧酸的酸性由强到弱排列为HClO>HClO2>HClO3>HClO4
A
【解析】
试题分析:A.H2O、H2S都是氧族元素形成的氢化物,结构相似,但是由于O元素的电负性大,原子半径小,所以在分子之间除了存在分子间作用力外,还存在氢键。增加了分子之间的相互作用,使得其熔沸点比与它相对分子质量大的H2S还高。正确。B.HF、HCl、HBr、HI也都是同族元素形成的氢化物。结构相似。一般情况下,结构相似的物质,相对分子质量越大,分子间的作用力就越大,物质的的熔点沸点就越高。但是由于F元素的电负性大,原子半径小,所以在分子之间除了存在分子间作用力外,还存在氢键。增加了分子之间的相互作用,使得其熔沸点要高很多。错误。C.乙醇分子与水分子之间除了存在范德华力外还存在氢键。错误。D.对同种元素形成的有氧酸之间的比较规律就是高价态的酸酸性强于低价态的酸的酸性。所以氯的各种含氧酸的酸性由强到弱排列为:HClO4> HClO3> HClO2>HClO。错误。
考点:考查物质的熔沸点与氢键的关系及同种元素形成的各种不同价态的含氧酸的酸性强弱的比较的知识。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
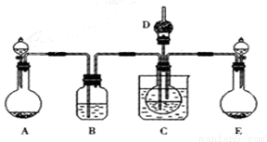

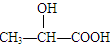 D.CH3CH2OH
D.CH3CH2OH