题目内容
对反应A(g)+3B(g)?2C(g)来说,下列反应速率中最快的是( )
| A、v(A)=0.3 mol?L-1?min-1 |
| B、v(B)=0.6 mol?L-1?s-1 |
| C、v(C)=0.5 mol?L-1?min-1 |
| D、v(A)=0.1 mol?L-1?s-1 |
考点:化学反应速率和化学计量数的关系
专题:化学反应速率专题
分析:不同物质表示的速率之比等于其化学计量数之比,故不同物质表示的速率与其化学计量数的比值越大,表示的反应速率越快,注意保持单位一致.
解答:
解:不同物质表示的速率之比等于其化学计量数之比,故不同物质表示的速率与其化学计量数的比值越大,表示的反应速率越快,对应反应:A(g)+3B(g)?2C(g),
A.
=0.3 mol?L-1?min-1;
B.v(A)=0.6 mol?L-1?s-1=36 mol?L-1?min-1,
=12 mol?L-1?s-1;
C.
=0.25 mol?L-1?min-1;
D.v(A)=0.1 mol?L-1?s-1=6 mol?L-1?min-1,
=6 mol?L-1?min-1;
故选B.
A.
| v(A) |
| 1 |
B.v(A)=0.6 mol?L-1?s-1=36 mol?L-1?min-1,
| v(B) |
| 3 |
C.
| v(C) |
| 2 |
D.v(A)=0.1 mol?L-1?s-1=6 mol?L-1?min-1,
| v(A) |
| 1 |
故选B.
点评:本题考查化学反应速率快慢比较,难度不大,利用比值法可以迅速判断,也可以转化为同一物质表示的速率进行比较.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
金属镁的密度较小,镁合金的强度高、机械性能好,是制造汽车、飞机、火箭的重要材料,从而获得“国防金属”的美誉.从化学原理和经济效益角度分析,下列海水中提取镁的方法最合理的是( )
A、海水
| |||||||||||
B、海水
| |||||||||||
C、海水
| |||||||||||
D、海水
|
把下列溶液加水稀释,溶液中每种离子的浓度都不会增加的是( )
| A、H2SO4溶液 |
| B、Na2SO4溶液 |
| C、Na2CO3溶液 |
| D、FeC13溶液 |
能用于治疗胃酸过多的是( )
| A、胃舒平[主要成分Al(OH)3] |
| B、阿司匹林 |
| C、青霉素 |
| D、烧碱 |
蛋白质发生的下列过程中,可逆的是( )
| A、变性 | B、煮熟 |
| C、盐析 | D、加入浓硫酸 |
关于如图所示的原电池,下列说法正确的是( )
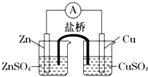

| A、锌是电池的负极,发生还原反应 |
| B、盐桥中的阳离子向硫酸铜溶液中迁移 |
| C、电流从锌电极通过检流计流向铜电极 |
| D、铜电极上发生的电极反应是2H++e-=H2↑ |
把V L含有KCl和BaCl2的混合溶液分成两等份,一份加入含a mol AgNO3的溶液,恰好使Cl-完全沉淀为AgCl;另一份加入含b mol Na2SO4的溶液,恰好使Ba2+完全沉淀为BaSO4.则原混合溶液中钾离子的浓度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
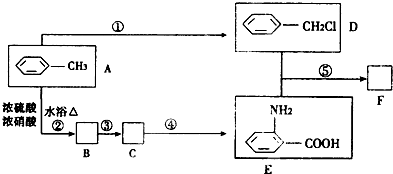
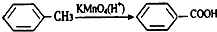
 (苯胺,弱碱性,易氧化)
(苯胺,弱碱性,易氧化)