题目内容
11.下列各示意图与对应的表述不正确的是( )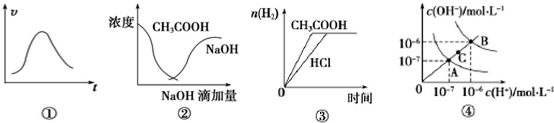
| A. | 图①可表示一定条件下,锌和稀硫酸反应的速率随时间变化的趋势图 | |
| B. | 图②中曲线表示将氢氧化钠溶液滴加到醋酸溶液中浓度的变化趋势图 | |
| C. | 图③表示等体积、等物质的量浓度的盐酸和醋酸,分别加足量镁粉,产生H2的物质的量变化 | |
| D. | 图④为水的电离平衡曲线图,若从A点到C点,可采用升高温度的方法 |
分析 A.锌和稀硫酸为放热反应,结合温度、浓度对反应速率的影响判断;
B.NaOH在醋酸消耗完之前是不会在溶液中存在的,NaOH的曲线向右平移,反应完全后滴入氢氧化钠,浓度会增大;
C.醋酸为弱酸,部分电离;
D.从A点到C点,氢离子和氢氧根离子浓度都增大.
解答 解:A.锌和稀硫酸为放热反应,开始反应温度升高,速率增大,随着反应进行,浓度较小,则反应速率减小,故A正确;
B.NaOH在醋酸消耗完之前是不会在溶液中存在的,NaOH的曲线向右平移,反应完全后滴入氢氧化钠,浓度会增大,故B正确;
C.等体积、等物质的量浓度的盐酸和醋酸溶液中,盐酸溶液中的氢离子浓度大,反应速率快,达到平衡所需时间少,最后生成氢气相同,故C错误;
D.从A点到C点,氢离子和氢氧根离子浓度都增大,水的离子积常数增大,则应为升高温度,故D正确.
故选C.
点评 本题考查较为综合,为高频考点和常见题型,侧重于学生的分析能力的考查,题目涉及反应速率影响因素分析,酸碱反应浓度变化图象分析判断,弱电解质除杂电离平衡,水溶液中离子积常数随温度变化,注意相关基础知识的积累,题目难度中等.

练习册系列答案
 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
1.实验室检验溶液中是否存在SO42-,可选用的化学试剂依次为( )
| A. | KCl(aq),HCl(aq) | B. | HNO3(aq),KNO3(aq) | C. | HCl(aq),BaCl2(aq) | D. | NaNO3(aq),HNO3(aq) |
2.已知氧化还原反应:2Cu(IO3)2+24KI+12H2SO4═2CuI↓+13I2+12K2SO4+12H2O,下列描述正确的是( )
| A. | I2仅是还原产物 | |
| B. | Cu(IO3)2既是氧化剂又是还原剂 | |
| C. | 氧化产物与还原产物物质的量比为13:2 | |
| D. | 当1 mol氧化剂参加反应时,被氧化的物质的物质的量为11mol |
19.某卤代烃与氢氧化钠的醇溶液在加热条件下反应产生丙烯,将剩余的溶液用硝酸酸化后,加入硝酸银溶液生成浅黄色沉淀.则原卤代烃的结构简式可能是( )
| A. | CH3CH2CH2-Cl | B. | 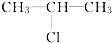 | C. | CH3CH2CH2-Br | D. | 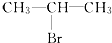 |
6.下列叙述错误的是( )
| A. | 同系物之间在化学性质上相似 | |
| B. | 同系物之间的物理性质随分子里碳原子数的递增,呈规律性的变化 | |
| C. | 同系物不可能是同分异构体 | |
| D. | 分子组成相差一个或几个CH2原子团的物质互称为同系物 |
16.25℃时,常见的无机酸在水溶液中的电离子平衡常数如表,下列选项正确的是( )
| 氢氰酸(HCN) | 碳酸(H2C03) | 氢氟酸(HF) |
| K=4.9×10-10 | K1=4.4×10-7 K2=4.7×10-11 | K=6.61×10-4 |
| A. | 氰化钠溶液中通入少量CO2:2CN-+H2O+CO2═2HCN+CO32- | |
| B. | NaCN与HCN的混合溶液中一定有:c(Na+)>c(CN-)>c(HCN)>c(H+)>c(OH+) | |
| C. | 0.2 mol•L-1 HCN溶液与0.1mol•L-1NaOH溶液等体积混合后,溶液中各种离子的浓度关系有:2[c(H+)-c(OH+)]=c(CN+)-c(HCN) | |
| D. | 等体积、等浓度的NaCN和NaF溶液中所含离子总数前者大于后者 |
3.将固体NH4I置于密闭容器中,在一定温度下发生下列反应:
①NH4I=NH3(g)+HI(g)
②2HI(g)=H2(g)+I2(g)
均为可逆反应,达到平衡时,c(H2)=0.5mol/L,c(HI)=4mol/L,则此温度下反应①的平衡常数为( )
①NH4I=NH3(g)+HI(g)
②2HI(g)=H2(g)+I2(g)
均为可逆反应,达到平衡时,c(H2)=0.5mol/L,c(HI)=4mol/L,则此温度下反应①的平衡常数为( )
| A. | 12mol2•L-2 | B. | 16mol2•L-2. | C. | 20mol2•L-2 | D. | 25mol2•L-2 |
20.对于放热反应H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl,下列说法中,正确的是( )
| A. | 生成物所具有的总能量高于反应物所具有的总能量 | |
| B. | 反应物所具有的总能量高于生成物所具有的总能量 | |
| C. | 断开1molH-H键和1molCl-Cl键所吸收的总能量大于形成2molH-Cl键所放出的能量 | |
| D. | 该反应中,化学能只转变为热能 |
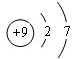 ,D离子的结构示意图:
,D离子的结构示意图: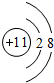 .
.