题目内容
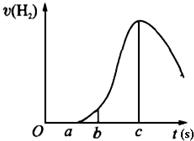 把在空气中久置的镁条7.2g投入盛有500mL 0.5mol?L-1硫酸溶液的烧杯中,镁条与硫酸反应产生氢气的速率与反应时间如图所示,回答下列问题:
把在空气中久置的镁条7.2g投入盛有500mL 0.5mol?L-1硫酸溶液的烧杯中,镁条与硫酸反应产生氢气的速率与反应时间如图所示,回答下列问题:(1)曲线由0→a段不产生氢气的原因
(2)曲线由b→c段,产生氢气的速率逐渐增大的主要原因
(3)曲线由c以后,产生氢气的速率逐渐下降的主要原因
(4)在b到c这段时间内,收集到氢气VL(标准状况),则这段时间内用硫酸表示的平均速率为
(5)对于足量镁条和100ml 2mol/L硫酸生成氢气的反应,下列措施能减缓反应速率,但又不影响生成氢气的总量的是
①加NaOH固体;②加BaCl2溶液;③加KNO3溶液;④加H2O;⑤加CH3COONa固体;⑥加小苏打溶液;⑦加少量CuSO4溶液;⑧加Na2SO4溶液;⑨将2mol/L硫酸换成160mL 2.5mol/L的盐酸;⑩将镁条换成镁粉.
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:(1)镁是活泼性较强的金属,能迅速和空气中的氧气反应生成氧化镁,根据氧化镁的性质分析;
(2)金属和酸的反应是放热反应,温度升高是影响反应速率的主要因素,根据温度对化学反应速率的影响分析;
(3)溶液的浓度是影响化学反应速率的主要因素;
(4)根据氢气的体积计算氢气的物质的量,进而确定HCl的物质的量,结合v=
计算反应速率;
(5)减缓反应速率,可降低浓度、温度,不影响生成氢气的总量,则氢离子的物质的量不变,以此解答.
(2)金属和酸的反应是放热反应,温度升高是影响反应速率的主要因素,根据温度对化学反应速率的影响分析;
(3)溶液的浓度是影响化学反应速率的主要因素;
(4)根据氢气的体积计算氢气的物质的量,进而确定HCl的物质的量,结合v=
| △c |
| △t |
(5)减缓反应速率,可降低浓度、温度,不影响生成氢气的总量,则氢离子的物质的量不变,以此解答.
解答:
解:(1)镁是活泼性较强的金属,能迅速和空气中的氧气反应生成氧化镁,氧化镁首先稀硫酸反应生成硫酸镁和水,不产生H2,离子方程式为MgO+2H+=Mg2++H2O,
故答案为:镁条表面有氧化镁,硫酸首先和与表面的氧化镁反应,不产生氢气;MgO+2H+=Mg2++H2O;
(2)金属和酸的反应是放热反应,使溶液的温度升高,温度升高是影响反应速率的主要因素,化学反应速率加快,
故答案为:镁和硫酸反应放出的热量使溶液温度升高而加快反应速率;
(3)随着反应的进行,溶液中的氢离子浓度逐渐降低,氢离子浓度是影响化学反应速率的主要因素,所以反应速率逐渐减小,
故答案为:随着反应的进行,硫酸的浓度逐渐变小,该因素变为影响反应速率的主要因素,使反应速率减小;
(4)n(H2)=
mol,则△n(H2SO4)=
mol,
v(H2SO4)=
=
mol/(L?s),
故答案为:
;
(5)减缓反应速率,可降低浓度、温度,不影响生成氢气的总量,则氢离子的物质的量不变,则符合要求的有②④⑤⑧⑨,
故答案为:②④⑤⑧⑨.
故答案为:镁条表面有氧化镁,硫酸首先和与表面的氧化镁反应,不产生氢气;MgO+2H+=Mg2++H2O;
(2)金属和酸的反应是放热反应,使溶液的温度升高,温度升高是影响反应速率的主要因素,化学反应速率加快,
故答案为:镁和硫酸反应放出的热量使溶液温度升高而加快反应速率;
(3)随着反应的进行,溶液中的氢离子浓度逐渐降低,氢离子浓度是影响化学反应速率的主要因素,所以反应速率逐渐减小,
故答案为:随着反应的进行,硫酸的浓度逐渐变小,该因素变为影响反应速率的主要因素,使反应速率减小;
(4)n(H2)=
| V |
| 22.4 |
| V |
| 22.4 |
v(H2SO4)=
| ||||
| (c-b)s |
| V |
| 11.2(c-b ) |
故答案为:
| V |
| 11.2(c-b ) |
(5)减缓反应速率,可降低浓度、温度,不影响生成氢气的总量,则氢离子的物质的量不变,则符合要求的有②④⑤⑧⑨,
故答案为:②④⑤⑧⑨.
点评:本题考查了化学反应速率的影响因素,难度不大,注意根据图象分析理解随反应进行影响反应速率的主导元素.

练习册系列答案
相关题目
某有机物结构简式为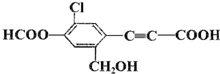 ,关于该有机物描述正确的是( )
,关于该有机物描述正确的是( )
 ,关于该有机物描述正确的是( )
,关于该有机物描述正确的是( )| A、该有机物分子式为:C11H5O5Cl |
| B、分子中最多有9个碳原子共平面 |
| C、1mol 该有机物分别与Na、NaOH、NaHCO3完全反应,消耗Na、NaOH、NaHCO3的物质的量依次为:2mol、5mol、1mol |
| D、该有机物不能发生银镜反应 |
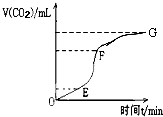 请用相关知识回答下列问题:
请用相关知识回答下列问题: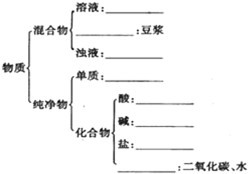 有下列物质:A.豆浆,B.食盐水,C.铁,D.硫酸,E.氢氧化钠固体,F.氯化钠,G.泥水,H.二氧化碳,I.水.请将它们的序号或所属类别填充到如图的横线上.(填写序号)
有下列物质:A.豆浆,B.食盐水,C.铁,D.硫酸,E.氢氧化钠固体,F.氯化钠,G.泥水,H.二氧化碳,I.水.请将它们的序号或所属类别填充到如图的横线上.(填写序号) Ⅰ.一定温度下,将3mol CO2和2mol H2混合于2L的密闭容器中,发生如下反应:C02(g)+H2(g)?CO(g)+H2O(g)
Ⅰ.一定温度下,将3mol CO2和2mol H2混合于2L的密闭容器中,发生如下反应:C02(g)+H2(g)?CO(g)+H2O(g)