题目内容
17.下列物质发生反应时其离子方程式正确的是( )| A. | 铁与三氯化铁溶液反应:Fe+2Fe3+=3Fe2+ | |
| B. | 氯化铝溶液中加入过量的氨水Al3++4NH3•H2O=4NH4++AlO2-+2H2O | |
| C. | Fe(OH)3跟盐酸反应:Fe(OH)3+3H+=Fe3++3H2O | |
| D. | 钠和冷水反应:Na+2H2O=Na++H2↑+2OH- |
分析 A.反应生成氯化亚铁,电子、电荷守恒;
B.反应生成氢氧化铝和氯化铵;
C.反应生成氯化铁和水;
D.反应生成NaOH和氢气,电子、电荷不守恒.
解答 解:A.铁与三氯化铁溶液反应的离子反应为Fe+2Fe3+=3Fe2+,故A正确;
B.氯化铝溶液中加入过量的氨水的离子反应为Al3++3NH3•H2O=3NH4++Al(OH)3↓,故B错误;
C.Fe(OH)3跟盐酸反应的离子反应为Fe(OH)3+3H+=Fe3++3H2O,故C正确;
D.钠和冷水反应的离子反应为2Na+2H2O=2Na++H2↑+2OH-,故D错误;
故选AC.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
相关题目
7.下列选用的仪器和药品不能达到实验目的是( )
| A | B | C | D |
 |  |  |  |
| 分离NH4Cl和Ca(OH)2固体 | X为四氯化碳,可用于吸收氨气,并防止倒吸 | 验证浓硫酸的脱水性和强氧化性 | 验证HCl气体在水中的溶解性 |
| A. | A | B. | B | C. | C | D. | D |
8.铜绿的主要成分为CuCO3•Cu(OH)2,下表中对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铜绿的主要成分是碱式碳酸铜 | 可用稀盐酸除铜器表面的铜绿 | Ⅰ对;Ⅱ对;有 |
| B | 铜表面易形成致密的氧化膜 | 铜容器可以盛放浓硫酸 | Ⅰ对;Ⅱ对;有 |
| C | 铁比铜活泼 | 铆在铜板上的铁钉在潮湿空气中不易生锈 | Ⅰ对;Ⅱ对;有 |
| D | 硫酸铜晶体受热转化为硫酸铜粉末属于风化过程 | 硫酸铜溶液可用作游泳池水的消毒 | Ⅰ错;Ⅱ对;无 |
| A. | A | B. | B | C. | C | D. | D |
5.氨水中的粒子数为( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
12.物质的量浓度相同的下列溶液中,符合按pH由小到大顺序排列的是( )
| A. | Na2CO3、NaHCO3、NaCl、NH4Cl | B. | Na2CO3、NaHCO3、NH4Cl、NaCl | ||
| C. | NH4Cl、(NH4)2SO4、Na2S、NaNO3 | D. | (NH4)2SO4、NH4Cl、NaNO3、Na2S |
 ,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H 6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H 6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
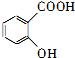 .
. .
. )为主要原料
)为主要原料 制备合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=CH2$\stackrel{Br_{2}}{→}$
制备合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$H2C=CH2$\stackrel{Br_{2}}{→}$ .
.