题目内容
在给定条件的水溶液中可能大量共存的离子组是( )
| A、c(H+):c(OH-)=1:2的溶液:K+、Al3+、HCO3-、ClO- |
| B、与Al反应生成H2的溶液:Na+、Ba2+、NO3-、Cl- |
| C、中性溶液中:SO32-、S2-、Fe3+、Cl- |
| D、能使红色酚酞变无色的溶液:K+、Ca2+、Cl-、HCO3- |
考点:离子共存问题
专题:
分析:A.c(H+):c(OH-)=1:2的溶液中,氢氧根离子大于氢离子,溶液显示弱碱性,铝离子与碳酸氢根离子、次氯酸根离子都发生双水解反应;
B.该溶液为酸性或者强碱性溶液,Na+、Ba2+、NO3-、Cl-离子之间不满足离子反应发生条件,且都不与氢离子和氢氧根离子反应;
C.铁离子能够氧化亚硫酸根离子、硫离子;
D.能使红色酚酞变无色的溶液为酸性溶液,碳酸氢根离子能够与氢离子反应生成二氧化碳气体.
B.该溶液为酸性或者强碱性溶液,Na+、Ba2+、NO3-、Cl-离子之间不满足离子反应发生条件,且都不与氢离子和氢氧根离子反应;
C.铁离子能够氧化亚硫酸根离子、硫离子;
D.能使红色酚酞变无色的溶液为酸性溶液,碳酸氢根离子能够与氢离子反应生成二氧化碳气体.
解答:
解:A.该溶液为弱碱性溶液,Al3+与HCO3-、ClO-之间发生双水解反应,在溶液中不能大量共存,故A错误;
B.与Al反应生成H2的溶液为酸性或碱性溶液,Na+、Ba2+、NO3-、Cl-离子之间不反应,都不与氢离子、氢氧根离子反应,在溶液中能够大量共存,故B正确;
C.SO32-、S2-都能够被Fe3+氧化,在溶液中不能大量共存,故C错误;
D.能使红色酚酞变无色的溶液中存在大量氢离子,HCO3-与氢离子反应生成二氧化碳和水,在溶液中不能大量共存,故D错误;
故选B.
B.与Al反应生成H2的溶液为酸性或碱性溶液,Na+、Ba2+、NO3-、Cl-离子之间不反应,都不与氢离子、氢氧根离子反应,在溶液中能够大量共存,故B正确;
C.SO32-、S2-都能够被Fe3+氧化,在溶液中不能大量共存,故C错误;
D.能使红色酚酞变无色的溶液中存在大量氢离子,HCO3-与氢离子反应生成二氧化碳和水,在溶液中不能大量共存,故D错误;
故选B.
点评:本题考查离子共存的正误判断,为高考中的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间等; 还需要注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;是“可能”共存,还是“一定”共存等.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
下列有关说法,不正确的是( )
①将盛有二氧化氮气体的试管倒立在水中,溶液会充满试管
②向煤中加入适量石灰石,在煤燃烧时最终生成CaSO4,可减少SO2对大气的污染
③为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化
④电解从海水中得到的氯化镁溶液可获得金属镁
⑤为证明NaHCO3溶液中混有Na2CO3,取少量溶液,加入澄清石灰水,若有白色沉淀生成,则证明混有Na2CO3.
①将盛有二氧化氮气体的试管倒立在水中,溶液会充满试管
②向煤中加入适量石灰石,在煤燃烧时最终生成CaSO4,可减少SO2对大气的污染
③为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化
④电解从海水中得到的氯化镁溶液可获得金属镁
⑤为证明NaHCO3溶液中混有Na2CO3,取少量溶液,加入澄清石灰水,若有白色沉淀生成,则证明混有Na2CO3.
| A、仅①③④⑤ | B、仅②③④ |
| C、仅①③④ | D、仅①②④⑤ |
在下列条件下,能大量共存的微粒组是( )
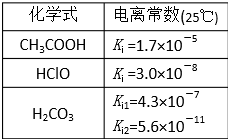

| A、c(H+)=1×10-14mol/L的溶液:K+、Na+、AlO2-、S2O32- |
| B、上表提供的数据下:HClO、HCO3-、ClO-、CO32- |
| C、能与Al反应生成H2的溶液:NH4+、Ca2+、NO3-、I- |
| D、中性的溶液中:CO32-、Na+、SO42-、AlO2- |
下列叙述正确的是( )
| A、电解质的电离是在通电的条件下进行的 |
| B、强电解质溶液的导电能力不一定比弱电解质溶液强 |
| C、盐酸是强电解质,所以盐酸中没有HCl分子 |
| D、H2O(g)═H2O(l)是放热反应 |
关于活化分子说法错误的是( )
| A、发生有效碰撞的分子一定是活化分子 |
| B、活化分子间的碰撞一定是有效碰撞 |
| C、能发生有效碰撞的分子必须具有相当高的能量 |
| D、使用催化剂能改变分子的活化能 |
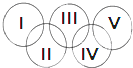 如右图,假定五环中的一环表示一种物质,相连环物质间一定条件下能发生常见反应,不相连环物质间不能发生反应,且四种反应中必须包含化合反应、置换反应及复分解反应,适合的一组是( )
如右图,假定五环中的一环表示一种物质,相连环物质间一定条件下能发生常见反应,不相连环物质间不能发生反应,且四种反应中必须包含化合反应、置换反应及复分解反应,适合的一组是( ) 已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-.向含3mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示.
已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-.向含3mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示. 有一瓶澄清溶液,其中可能含有NH4+、K+、Ba2+、Al3+、Fe3+、Mg2+、I-、NO3-、CO32-、SO42-、AlO2-.取该溶液进行以下实验:
有一瓶澄清溶液,其中可能含有NH4+、K+、Ba2+、Al3+、Fe3+、Mg2+、I-、NO3-、CO32-、SO42-、AlO2-.取该溶液进行以下实验: