题目内容
12.氮在自然界的循环过程中可发生反应:N2+O2 $\frac{\underline{\;放电\;}}{\;}$2NO.该反应中,被还原的物质是O2(填化学式),作为还原剂的物质是N2(填化学式);若反应中消耗1mol N2,则生成NO2mol.分析 在氧化还原反应中,得电子化合价降低的反应物是氧化剂,失电子化合价升高的反应物是还原剂,还原剂被氧化,根据原子守恒计算生成NO的物质的量.
解答 解:该反应中,N元素化合价由0价变为+2价、O元素化合价由0价变为-2价,所以是氧化剂O2,N2是还原剂,被氧化的物质是N2,若反应中消耗了1mol N2,根据N原子守恒知,生成2molNO,
故答案为:O2;N2;2.
点评 本题考查了氧化还原反应,根据氧化剂、还原剂的概念结合原子守恒来分析解答即可,熟悉常见元素的化合价,题目难度不大.

练习册系列答案
相关题目
2.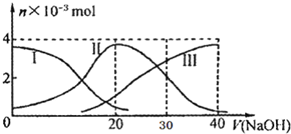 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HA-,III代表A2-),根据图示判断,下列说法不正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HA-,III代表A2-),根据图示判断,下列说法不正确的是( )
 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HA-,III代表A2-),根据图示判断,下列说法不正确的是( )
常温下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有关微粒的物质的量变化如图(其中I代表H2A,II代表HA-,III代表A2-),根据图示判断,下列说法不正确的是( )| A. | H2A在水中的电离方程式是:H2A═H++HA-;HA-═H++A2- | |
| B. | 当V(NaOH)=20mL时,溶液中各粒子浓度的大小顺序为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) | |
| C. | 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水小 | |
| D. | 当V(NaOH)=30mL时,溶液中存在以下关系:2c(H+)+c(HA-)+2c(H2A)=c(A2-)+2 c(OH-) |
3.下列晶体中,可能具有层状晶体的是( )
| A. | CaF2 | B. | Na2O | C. | CuSO4•5H2O | D. | FeCl3 |
20.羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫的危害.在恒容密闭容器中,CO和H2S混合加热生成羰基硫的反应为 CO(g)+H2S(g)?COS(g)+H2(g).下列说法能充分说明该反应已经达到化学平衡状态的是( )
| A. | 正、逆反应速率都等于零 | B. | CO、H2S、COS、H2的浓度相等 | ||
| C. | CO、H2S、COS、H2在容器中共存 | D. | CO、H2S、COS、H2的浓度均不再变化 |
7.在实验室和生产生活中,安全都是避免伤害和事故的保障.下列安全问题的处理方法不正确的是( )
| A. | 金属钠着火时立即用沙子盖灭 | |
| B. | 将过期的化学药品直接倒入下水道 | |
| C. | 少量浓硫酸溅到皮肤上立即用大量水冲洗 | |
| D. | 用肥皂液涂在天然气管道接口处检验是否漏气 |
4.下列物质久置于敞口容器中,不易变质的是( )
| A. | 次氯酸 | B. | 金属钠 | C. | 氯化钠 | D. | 氧化钙 |
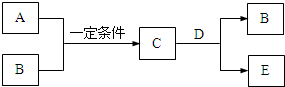 A、B、C、D、E是中学化学中的常见物质,A、B是短周期元素组成的单质.其转化关系如图:
A、B、C、D、E是中学化学中的常见物质,A、B是短周期元素组成的单质.其转化关系如图: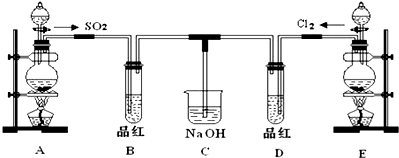
 ;请指出该反应中的液体反应物在反应中所表现出的化学性质:还原性和酸性;若液体中的溶质反应了6mol,则转移的电子的物质的量3mol;
;请指出该反应中的液体反应物在反应中所表现出的化学性质:还原性和酸性;若液体中的溶质反应了6mol,则转移的电子的物质的量3mol;