题目内容
13.下列各组物质中化学键的类型相同的是( )| A. | HCl MgCl2 NH4Cl | B. | H2O Na2O CO2 | ||
| C. | CaCl2 NaOH H2O | D. | NH3 H2O CO2 |
分析 一般来说,活泼金属和活泼非金属元素易形成离子键,非金属元素之间易形成共价键,以此来解答.
解答 解:A.氯化氢含有H-Cl共价键,氯化镁含有离子键,氯化铵含有离子键、N-H共价键,故A不选;
B.水中含有H-O共价键,氧化钠含有离子键,二氧化碳中存在C=O共价键,故B不选;
C.氯化钙中含有离子键,氢氧化钠含离子键和O-H共价键,故C不选;
D.NH3含有N-H共价键、H2O中含有H-O共价键,二氧化碳中含有C=O共价键,所以三种物质所含有化学键都是共价键,类型相同,故D选;
故选:D.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
4.已知在1×105 Pa、298K条件下,2mol氢气燃烧生成水蒸气,放出484kJ热量,下列热化学方程式正确的是( )
| A. | H2O(g)═H2(g)+$\frac{1}{2}$O2(g)△H=-242 kJ/mol | B. | 2H2(g)+O2(g)═2H2O(l)△H=-484 kJ/mol | ||
| C. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-242 kJ/mol | D. | 2H2(g)+O2(g)═2H2O(g)△H=+484 kJ/mol |
1.下列表示对应化学反应的离子方程式正确的是( )
| A. | 用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- | |
| B. | 向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 用惰性电极电解CuSO4溶液:2Cu2++2H2O═4H++O2↑+2Cu | |
| D. | Cu溶于稀硝酸HNO3:Cu+2H++NO3-═Cu2++NO2↑+H2O |
2.2015年9月18日,美国环保署EPA宣布,大众汽车公司利用软件隐瞒了汽车有毒污染物的真实排放量.汽车尾气中的污染物有固体悬浮微粒、一氧化碳、碳氢化合物、氮氧化合物、铅及硫氧化合物等.下列有关说法正确的是( )
| A. | 一氧化碳、氮氧化物是酸雨形成的主要因素 | |
| B. | 汽车尾气可通过净化装置将碳氢化合物还原成CO2和H2O | |
| C. | 含铅化合物导致人体蛋白质变性是物理变化 | |
| D. | 固体悬浮微粒是造成雾霾天气的一种重要因素 |
6.中国药学家屠呦呦荣获2015年诺贝尔生理学或医学奖,成为首位获得诺贝尔科学类奖项的中国人.获奖理由是她发现了抗疟新药--青蒿素.青蒿素的分子是为C15H22O5,常温下是一种无色针状晶片.下列有关说法正确的是( )

| A. | 青蒿素属于无机化合物 | |
| B. | 青蒿素属于氧化物 | |
| C. | 标准状况下,1mol青蒿素的体积约为22.4L | |
| D. | 青蒿素的摩尔质量为282g/mol |
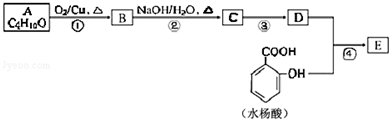
 ;
;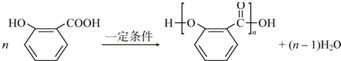 .
.