题目内容
从海水中提取溴有如下反应5NaBr+NaBrO3+3H2SO4═3Br2+3Na2SO4+3H2O.与上述反应在氧化还原原理上最相似的是( )
| A、2NaBr+Cl2═2NaCl+Br2 |
| B、AlCl3+3NaAlO2+6H2O═4Al(OH)3↓+3NaCl |
| C、2H2S+SO2═3S↓+2H2O |
| D、2FeCl3+H2S═2FeCl2+2HCl+S↓ |
考点:氧化还原反应
专题:氧化还原反应专题
分析:题干中的反应为氧化还原反应,只有溴元素的化合价发生变化,高价+5价和低价-1价均变为0价的一种氧化还原反应,属于氧化还原反应中的归中反应类型.
解答:
解:A、化合价变化的分别是溴元素和氯元素,不是归中反应类型,故A错误;
B、反应中没有元素化合价的变化,不是氧化还原反应,故B错误;
C、硫元素的化合价从-2价升到0价,还有的从+4价降到0价,属于氧化还原反应中的归中反应类型,故C正确;
D、化合价变化的分别是铁元素和硫元素,不是归中反应类型,故D错误;
故选C.
B、反应中没有元素化合价的变化,不是氧化还原反应,故B错误;
C、硫元素的化合价从-2价升到0价,还有的从+4价降到0价,属于氧化还原反应中的归中反应类型,故C正确;
D、化合价变化的分别是铁元素和硫元素,不是归中反应类型,故D错误;
故选C.
点评:本题考查学生氧化还原反应知识,侧重于考查学生分析和解决问题的能力,难度不大,注意把握氧化还原反应中的归中反应.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列解释事实的方程式不正确的是( )
| A、测0.1 mol/L的氨水的pH为11:NH3?H2O?NH4++OH- | ||||
| B、将Na块放入水中,产生气体:2Na+2H2O═2OH-+2Na++H2↑ | ||||
| C、Al片溶于NaOH溶液中,产生气体:2Al+2OH-+2H2O═2AlO2-+3H2↑ | ||||
D、用CuCl2溶液做导电性实验,灯泡发光:CuCl2
|
PCl3和PCl5都是重要的化工原料.将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中,在一定条件下
发生下述反应,并于10min时达到平衡:PCl3(g)+Cl2(g)?PCl5(g).有关数据如表所示.则有关判断不正确的是( )
发生下述反应,并于10min时达到平衡:PCl3(g)+Cl2(g)?PCl5(g).有关数据如表所示.则有关判断不正确的是( )
| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度/(mol/L) | 2.0 | 1.0 | 0 |
| 平衡浓度/(mol/L) | c1 | c2 | 0.4 |
| A、10 min内,v(Cl2)=0.04mol/(L?min) |
| B、升高温度,反应的平衡常数减小,则平衡时PCl3的转化率变大 |
| C、当容器中Cl2为1.2mol时,反应达到平衡 |
| D、平衡后移走2.0mol PCl3和1.0mol Cl2,在相同条件下再达平衡时,c(PCl5)<0.2mol/L |
在标准状况下,将V L A气体(摩尔质量M g/mol)溶于100ml水中(A与水不反应),所得A的水溶液密度为ρ g/cm3,则此溶液的物质的量浓度(mol/L)为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
有机物的种类繁多,但其命中是有规则的.下列有机物命名正确的是( )
A、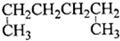 1,4-二甲基丁烷 1,4-二甲基丁烷 |
B、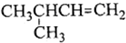 3-甲基丁烯 3-甲基丁烯 |
C、 2-甲基丁烷 2-甲基丁烷 |
| D、CH2Cl-CH2Cl 二氯乙烷 |
下列说法正确的是( )
| A、甲苯分子中所有原子都处于同一平面内 |
| B、1个苯分子中含有3个碳碳双键 |
| C、乙烯和苯都能使溴水褪色,褪色的原理相同 |
| D、100 g质量分数为46%的乙醇溶液中,共有14 mol共价键 |
某学生测定CuSO4?xH2O晶体的x值,数据如下(已知x的理论值为5.0):
产生误差的可能原因是( )
| 坩埚质量 | 坩埚+试样 | 失水后,坩埚+试样 |
| 11.70g | 20.82g | 16.02g |
| A、硫酸铜晶体中含不挥发杂质 |
| B、加热时有晶体溅出 |
| C、实验前,晶体表面有吸附水 |
| D、未做恒重操作 |
某温度时,在体积为1L的密闭容器中,A、B、C三种气体浓度的变化如图I所示,若其它条件不变,当温度分别为Tl和T2时,B的体积百分含量与时间关系如图Ⅱ所示.则下列结论正确的是( )
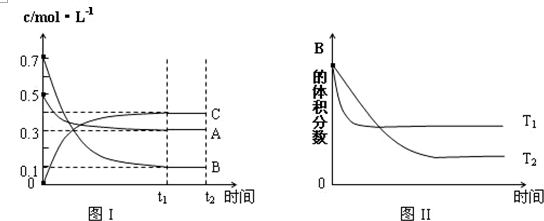

| A、该反应的热化学方程式为:A(g )+3B(g)?2C(g);△H>0 |
| B、达到平衡后,若其他条件不变,通入稀有气体,平衡向正反应方向移动 |
| C、达到平衡后,若其他条件不变,减小体积,平衡向逆反应方向移动 |
| D、若其它条件不变,升高温度,正、逆反应速率均增大,A的转化率减小 |