题目内容
14.NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | .常温常压下,18 g H2O中含有的电子总数为10NA | |
| B. | .1 mol•L-1 NaCl溶液含有NA个Na+ | |
| C. | 常温常压下,92 g的NO2和N2O4混合气体含有的原子数为3 NA | |
| D. | 标准状况下,2.24LCH4所含中子数为NA |
分析 A.依据n=$\frac{m}{M}$计算水的物质的量,结合1mol水含有10个电子;
B.溶液体积未知;
C.NO2和N2O4最简式相同为NO2,计算92gNO2中所含原子数;
D.1个甲烷分子含有6个中子.
解答 解:A.常温常压下,18 g H2O中含有的电子总数为$\frac{18g}{18g/mol}$×10×NA=10NA,故A正确;
B.溶液体积未知,无法计算溶液中钠离子个数,故B错误;
C.NO2和N2O4最简式相同为NO2,计算92gNO2中所含原子数=$\frac{92g}{46g/mol}$×3×NA=6NA,故C错误;
D.标准状况下,2.24LCH4物质的量为$\frac{2.24L}{22.4L/mol}$=0.1mol,含中子数为0.6NA,故D错误;
故选:A.
点评 本题考查阿伏加德罗常数的有关计算和判断,熟练掌握以物质的量为中心的各化学量与阿伏加德罗常数的关系是解题关键,注意物质的结构组成,题目难度不大.

练习册系列答案
相关题目
4.下列反应不属于氧化还原反应的是( )
| A. | 3Cl2+6KOH═5KCl+KClO3+3H2O | B. | 2NO2+2NaOH═NaNO3+NaNO2+H2O | ||
| C. | Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 | D. | SnCl4+2H2O═SnO2+4HCl |
5.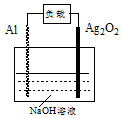 铝-氧化银电池是一种可供重型鱼雷使用的军用电池,4Al+3Ag2O2=2Al2O3+6Ag. 下列说法正确的是( )
铝-氧化银电池是一种可供重型鱼雷使用的军用电池,4Al+3Ag2O2=2Al2O3+6Ag. 下列说法正确的是( )
 铝-氧化银电池是一种可供重型鱼雷使用的军用电池,4Al+3Ag2O2=2Al2O3+6Ag. 下列说法正确的是( )
铝-氧化银电池是一种可供重型鱼雷使用的军用电池,4Al+3Ag2O2=2Al2O3+6Ag. 下列说法正确的是( )| A. | Ag2O2 为电池的正极 | B. | NaOH溶液为电解质溶液 | ||
| C. | 电池工作时,OH-向正极移动 | D. | 电池工作时,电能转变为化学能 |
2.下列说法中正确的是( )
| A. | 物质的量是国际单位制中的七个基本物理量之一 | |
| B. | 物质的量实质上就是物质的数量 | |
| C. | 常用6.02×1023表示阿伏伽德罗常数 | |
| D. | 阿伏伽德罗常数是12g碳中所含的碳原子数 |
9.下列各晶体熔沸点高低的比较,正确的是( )
| A. | H2O>NH3>H2 | B. | CsCl>KCl>NaCl | ||
| C. | SiO2>CO2>Hg | D. | 硅>金刚石>石英砂 |
18.有关下列离子方程式的说法正确的是( )
| A. | 向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| B. | 向NaAlO2溶液中通入少量的CO2的反应为:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- | |
| C. | FeBr2与足量的Cl2反应为:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | |
| D. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
 氢能是一种极具发展潜力的清洁能源.
氢能是一种极具发展潜力的清洁能源.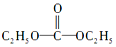 ,则碳酰肼的结构简式为
,则碳酰肼的结构简式为 .
.