题目内容
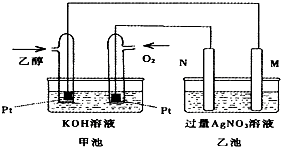 如图是一个乙醇燃料电池常温工作原理示意图,乙池中的两个电极一个是石墨电极,一个是铁电极.工作时M、N两个电极的质量都不减少,则下列说法正确的是( )
如图是一个乙醇燃料电池常温工作原理示意图,乙池中的两个电极一个是石墨电极,一个是铁电极.工作时M、N两个电极的质量都不减少,则下列说法正确的是( )| A、M电极的材料是石墨 |
| B、若乙池中某一电极质量增加4.32g时,理论上消耗氧气为448ml |
| C、在此过程中,甲池中OH-向通乙醇的一极移动 |
| D、在此过程中,乙池溶液中电子从M电极向N电极移动 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:乙醇燃料电池中,通入乙醇的电极是负极发生氧化反应,通入氧气的电极为正极发生还原反应,M为阴极,N为阳极,两极质量都不减少,说明铁做阴极,据离子放电顺序分析电解产物.
解答:
解:A、M为阴极,N为阳极,两极质量都不减少,说明铁做阴极,M电极材料为铁,故A错误;
B、乙池是电解池,阴极电极反应式为Ag++e-=Ag,质量增加4.32g为0.04mol,转移电子0.04mol,正极电极反应式为2H2O+O2+4e-=4OH-,转移0.04mol电子,需要氧气0.01mol,标准状况下体积为224mL,故B错误;
C、在原电池中,阴离子移向负极,乙醇在负极反应,故C正确;
D、溶液中离子定向移动形成电流,电子在电极和外电路中移动,不能在溶液中移动,故D错误;
故选C.
B、乙池是电解池,阴极电极反应式为Ag++e-=Ag,质量增加4.32g为0.04mol,转移电子0.04mol,正极电极反应式为2H2O+O2+4e-=4OH-,转移0.04mol电子,需要氧气0.01mol,标准状况下体积为224mL,故B错误;
C、在原电池中,阴离子移向负极,乙醇在负极反应,故C正确;
D、溶液中离子定向移动形成电流,电子在电极和外电路中移动,不能在溶液中移动,故D错误;
故选C.
点评:本题考查了原电池原理和电解池原理的应用,注意根据串联电路中转移的电子的物质的量相等结合电极方程式计算分析,题目难度中等.

练习册系列答案
相关题目
常温下,取pH均等于2的盐酸和醋酸各100mL分别稀释10倍后,再分别加入0.03g锌粉,在相同条件下充分反应,有关叙述正确的是( )
| A、醋酸与锌反应放出的氢气多 |
| B、盐酸与锌反应放出的氢气多 |
| C、醋酸与锌反应的速率大 |
| D、盐酸和醋酸分别与锌反应速率一样大 |
下列反应属于吸热反应的是( )
| A、C6H12O6(葡萄糖)+6O2→6CO2+6H2O |
| B、CH3COOH+KOH═CH3COOK+H2O |
| C、Mg与HCl反应生成H2 |
| D、胆矾加热变为白色粉末 |
短周期元素W、X、Y、Z的原子序数依次增大,其简单离子不能破坏水的电离平衡的是( )
| A、W- |
| B、X+ |
| C、Y3+ |
| D、Z2- |
下列化学用语书写正确的是( )
A、甲烷的电子式: |
B、丙烯的键线式: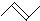 |
C、乙醚的结构式: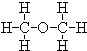 |
| D、乙烯的结构简式:CH2CH2 |