题目内容
15.溶质都为1mol的NaHCO3溶液和Ba(OH)2溶液混合,能完整表示该反应的离子方程式是( )| A. | CO32-+Ba2+=BaCO3 | |
| B. | HCO3-+OH-→H2O+CO32- | |
| C. | HCO3-+Ba2++OH-→H2O+BaCO3 | |
| D. | 2HCO3-+Ba2++OH-=BaCO3+2H2O+CO32- |
分析 NaHCO3和Ba(OH)2的相等,氢氧根离子过量,反应生成碳酸钡沉淀、氢氧化钠和水,据此书写离子方程式.
解答 解:溶质都为1mol的NaHCO3溶液和Ba(OH)2溶液混合,氢氧根离子过量,反应生成碳酸钡、NaOH和水,反应的离子方程式为HCO3-+Ba2++OH-=H2O+BaCO3,
故选C.
点评 本题考查离子方程式的书写,题目难度不大,明确发生反应的实质为解答关键,注意熟练掌握离子方程式的书写原则,试题有利于提高学生的灵活应用能力.

练习册系列答案
相关题目
3.一定条件下,对于可逆反应X(g)+3Y(g)?2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3 (均不为零),平衡时 X、Y、Z 的浓度分别为 0.1mol/L、0.3mol/L、0.08mol/L,则下列判断正确的( )
| A. | c1:c2=3:1 | |
| B. | 平衡时.Y和Z的生成速率之比为2:3 | |
| C. | X、Y的转化率不相等 | |
| D. | c1 的取值范围为 0 mol/L<c1<0.14 mol/L |
20.X、Y、Z、R、W是原子序数依次增大的五种短周期元素.Y和R同主族,可组成共价化合物RY2,Y和Z最外层电子数之和与W的最外层电子数相同,25℃时,0.1mol/LX和W形成化合物的水溶液pH=1.下列说法正确的是( )
| A. | Z与Y、Z与W形成的化合物的化学键完全相同 | |
| B. | X与Y组成的简单氢化物的沸点高于X与R组成的简单氢化物的沸点,是因为非金属性Y>R | |
| C. | 简单离子的半径:Z>R>W>Y | |
| D. | Y、Z、W三种元素组成的化合物的水溶液可能显碱性 |
7.W、X、Y、Z均是短周期元素,X、Y、Z处于同一周期,W、X、Z的简单离子具有相同的电子层结构,W的最高氧化物的水化物可与其最简单的气态氢化物反应生成易溶于水的盐,X的氧化物具有两性,Y的最高正价与最低负价的代数和为0,下列说法正确的是( )
| A. | 离子半径:W>Z>X | |
| B. | 单质熔点:W>Z | |
| C. | 最高正价:W>X>Y>Z | |
| D. | W、X、Z最高价氧化物对应的水化物相互之间能发生反应 |
5.X、Y、Z、W为原子序数依次增大的四种第三周期元素,其单质及其化合物的性质或结构信息如表所示,用化学用语回答下列问题.
请按要求回答下列问题:
(1)工业上制取X的单质的化学方程式:MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑.
(2)X、Y、W三种元素对应的离子半径由大到小的顺序为:Cl->Mg2+>Al3+.
(3)在25℃、101kPa下,已知13.5g的Y的固体单质在W的气体单质中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式是2Al(s)+3Cl2(g)=2AlCl3(s)△H=-1676kJ/mol.
(4)甲中各原子都满足8电子稳定结构,其电子式为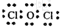 ;
;
(5)Sn与元素Z同主族,周期数比元素Z的大2.则Sn的原子序数为50;已知锡在水溶液中有Sn2+、Sn4+两种存在形式,且硫酸盐均可溶.酸性条件下,SnSO4可用作双氧水的去除剂,试写出所发生反应的离子方程式:Sn2++H2O2+2H+═Sn4++2H2O.潮湿环境中,镀锡铜如果锡层破损不能(填“能”或“不能”)形成铜绿.
| 元素 | X | Y | Z | W |
| 性质 结构 信息 | 工业上常用电解熔融XW2制取X的单质. | Y的最外层电子数比最内层电子数多1. | Z的最高价氧化物的水化物经聚合、脱水,可作袋装食品干燥剂. | W的一种气态氧化物甲对空气的相对密度为3,它溶于水得到单一溶质的弱酸性溶液(有漂白性),该溶液光照后酸性增强. |
(1)工业上制取X的单质的化学方程式:MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑.
(2)X、Y、W三种元素对应的离子半径由大到小的顺序为:Cl->Mg2+>Al3+.
(3)在25℃、101kPa下,已知13.5g的Y的固体单质在W的气体单质中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式是2Al(s)+3Cl2(g)=2AlCl3(s)△H=-1676kJ/mol.
(4)甲中各原子都满足8电子稳定结构,其电子式为
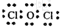 ;
;(5)Sn与元素Z同主族,周期数比元素Z的大2.则Sn的原子序数为50;已知锡在水溶液中有Sn2+、Sn4+两种存在形式,且硫酸盐均可溶.酸性条件下,SnSO4可用作双氧水的去除剂,试写出所发生反应的离子方程式:Sn2++H2O2+2H+═Sn4++2H2O.潮湿环境中,镀锡铜如果锡层破损不能(填“能”或“不能”)形成铜绿.

 某研究性学习小组为探究锌与盐酸反应,取同质量、同体积的锌片、同浓度盐酸做了下列平行实验:
某研究性学习小组为探究锌与盐酸反应,取同质量、同体积的锌片、同浓度盐酸做了下列平行实验: 铜和稀硝酸反应时,会出现奇妙的速率变化,开始时二者的反应速率非常慢,但随着反应的进行,反应速率却逐渐明显加快.对于上述变化的原因,课外活动小组同学进行了实验探究.
铜和稀硝酸反应时,会出现奇妙的速率变化,开始时二者的反应速率非常慢,但随着反应的进行,反应速率却逐渐明显加快.对于上述变化的原因,课外活动小组同学进行了实验探究.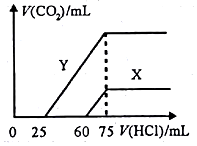 A、B、C、D、E、F是分属三个短周期的主族元素,且原子序数依次增大.A、D同主族,B的氢化物水溶液呈碱性,C、E同主族,形成的化合物EC2是形成酸雨的主要物质之一.请化学用语回答下列问题:
A、B、C、D、E、F是分属三个短周期的主族元素,且原子序数依次增大.A、D同主族,B的氢化物水溶液呈碱性,C、E同主族,形成的化合物EC2是形成酸雨的主要物质之一.请化学用语回答下列问题: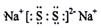 ,写出在空气中长期放置生成H的化学反应方程式为:4Na2S+O2+2H2O=4NaOH+2Na2S2.H的溶液与稀硫酸反应产生的现象为溶液由黄色变为无色,产生浅黄色沉淀和气体产生.
,写出在空气中长期放置生成H的化学反应方程式为:4Na2S+O2+2H2O=4NaOH+2Na2S2.H的溶液与稀硫酸反应产生的现象为溶液由黄色变为无色,产生浅黄色沉淀和气体产生.