题目内容
10.将0.2mol两种气态烃组成的混合气完全燃烧后得到6.72L CO2 (标准状况下)和7.2g水,下列说法正确的是( )| A. | 一定有乙烯 | B. | 一定没有乙烯 | C. | 一定有甲烷 | D. | 可能有乙烷 |
分析 由n=$\frac{m}{M}$计算7.2克水的物质的量,由n=$\frac{V}{Vm}$计算二氧化碳的物质的量,根据H原子、C原子守恒计算混合物的平均分子组成,以此来解答.
解答 解:两种气态烃组成的混合物0.2mol完全燃烧得6.72L二氧化碳和7.2克水,
7.2克水的物质的量为$\frac{7.2g}{18g/mol}$=0.4mol,平均分子组成中H原子数目为$\frac{0.4mol×2}{0.2mol}$=4,
6.72L二氧化碳的物质的量为$\frac{6.72L}{22.4L/mol}$=0.3mol,平均分子组成C原子数目为$\frac{0.3mol}{0.2mol}$=1.5,
故该混合烃的平均分子式为C1.5H4,
根据碳原子可知,该烃一定含有CH4,根据H原子可知,另一烃的分子中H原子数目为4,可能含乙烯、丙炔,一定不含乙烷,
故选C.
点评 本题考查有机物分子式的确定,为高频考点,把握物质的量的相关计算、平均值法、原子守恒为解答的关键,侧重分析与应用能力的考查,注意甲烷的确定方法,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.下列化学式及结构式中,从成键情况看不合理的是( )
| A. | CH3N, | B. | CH4Si, | C. | CH2SO, | D. | CH4S,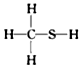 |
18.下列有机物发生的反应属于加成反应的是( )
| A. | 乙烯使KMnO4溶液褪色 | B. | 用乙醇、乙酸与浓H2SO4混合加热 | ||
| C. | 乙烯使溴的四氯化碳溶液褪色 | D. | 甲烷和氯水混合,见光 |
15.光照对下列反应(或变化)几乎没有影响的是( )
| A. | 浓硝酸由无色变黄色 | B. | 新制氯水变质 | ||
| C. | 甲烷与氯气反应 | D. | 苯与溴单质反应 |
2.关于原子轨道的说法正确的是( )
| A. | 凡是中心原子采取sp3杂化轨道成键的分子其几何构型都是正四面体 | |
| B. | 1个原子轨道里最多只能容纳2个电子,但自旋方向相同 | |
| C. | sp3杂化轨道是由同一个原子中能量相近的s轨道和p轨道混合起来形成的一组新轨道 | |
| D. | 凡AB3型的共价化合物,其中的中心原子A均采用sp3杂化轨道成键 |
18.某有机物的结构简式为HO-CH2CH=CH-COOH,该有机物不可能发生的化学反应是( )
| A. | 水解 | B. | 酯化 | C. | 加成 | D. | 氧化 |
17.伦敦奥运火炬彩用的是环保型燃料--丙烷,其燃烧时发生反应的化学方程式为C3H8+5O2$\frac{\underline{\;点燃\;}}{\;}$3CO2+4H2O.下列说法中不正确的是( )
| A. | 火炬燃烧时化学能只转化为热能 | |
| B. | 所有的燃烧反应都会释放热量 | |
| C. | 1 mol C3H8和5 mol O2所具有的总能量大于3 mol CO2和4 mol H2O所具有的总能量 | |
| D. | 丙烷完全燃烧的产物对环境无污染,故丙烷为环保型燃料 |
 ;
; .
.