题目内容
喜树中含有一种被称为喜树碱的生物碱,这种碱的相对分子质量在300~400之间,实验分析得知其元素组成为:C占69.0%、O占18.4%,且O含量为H的4倍,其余为N,则一个喜树碱分子中含有的原子总数为( )
| A、42 | B、43 | C、44 | D、45 |
考点:物质分子中的原子个数计算
专题:计算题
分析:根据元素的含量来计算物质的化学式,然后利用化学式可知物质的构成,则可判断分子中的原子总数.
解答:
解:由O占18.4%,且O含量为H的4倍,则H元素的含量为4.6%,
N元素的含量为1-69%-4.6%-18.4%=8%,
则该物质中C、H、O、N的原子个数比为
:
:
:
=10:8:2:1,
则该物质的化学式为(C10H8O2N)n,
又碱的相对分子质量在300~400之间,
300<(12×10+1×8+16×2+14)×n<400,
则n=2符合,
即物质的化学式为C20H16O4N2,
则1个分子中含有20+16+4+2=42个原子,
故选A.
N元素的含量为1-69%-4.6%-18.4%=8%,
则该物质中C、H、O、N的原子个数比为
| 69.0% |
| 12 |
| 4.6% |
| 1 |
| 18.4% |
| 16 |
| 8% |
| 14 |
则该物质的化学式为(C10H8O2N)n,
又碱的相对分子质量在300~400之间,
300<(12×10+1×8+16×2+14)×n<400,
则n=2符合,
即物质的化学式为C20H16O4N2,
则1个分子中含有20+16+4+2=42个原子,
故选A.
点评:本题考查学生利用元素的质量分数来计算得出物质的化学式,再利用化学式判断物质的构成即可解答,计算较复杂,题目难度不大.

练习册系列答案
相关题目
在恒温、恒容的密闭容器中进行反应B(g)+C(g)?A(g),若反应物B的浓度由2mol?L-1降到0.8mol?L-1需要时间ts,该反应物再由0.8mol?L-1降到0.2mol?L-1所需要的时间为5s,则t为( )
| A、小于10s | B、10s |
| C、大于10s | D、无法判断 |
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、标准状况下2.24L氯气通入水中,电子转移数为0.1NA |
| B、6.8g熔融的KHSO4中含有0.1Na个阳离子 |
| C、CO和N2为等电子体,22.4L的CO气体与NA 个N2所含的电子数相等 |
| D、0.6 g CaCO3与Mg3N2的混合物中所含质子数为0.3NA |
汶川“5?12”大地震震惊全球,一些化工厂受地震影响相继发生过氨气泄漏事故和重大液氯泄漏事故,幸好部队抢险及时,避免了人民生命财产的损失.下列有关氯气和氨气的说法正确的是( )
| A、氯气和氨气都是由极性键构成的分子 |
| B、氯气和氨气都是无色、密度比空气大的有毒气体 |
| C、氯气和氨气都是易液化的气体 |
| D、氯气和氨气分子中所有原子都满足最外层为8电子结构 |
短周期元素W、X、Y、Z的原子序数依次增大,W与Y、X与Z位于同一主族,W与X可形成共价化合物WX2,Y原子的内层电子总数是其最外层电子数的2.5倍.下列叙述中不正确的是( )
| A、WZ2分子中所有原子最外层都为8电子结构 |
| B、原子半径大小顺序为X<W<Y<Z |
| C、WX2、ZX2水溶液呈酸性,都能导致酸雨 |
| D、WX2是以极性键结合成的非极性分子 |
用下列实验装置完成对应的实验(部分仪器已省略),操作正确并能达到实验目的是( )
A、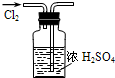 干燥Cl2 |
B、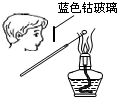 检验K2CO3中的K+ |
C、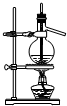 石油的蒸馏 |
D、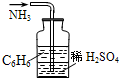 吸收NH3 |
“拟晶”(quasicrystal)是一种具有凸多面体规则外形但不同于晶体的固态物质.A165Cu23Fel2是二十世纪发现的几百种拟晶之一,具有合金的某些优良物理性能.有关这种拟晶的说法错误的是( )
| A、A165Cu23Fel2的硬度比金属A1、Cu、Fe都大 |
| B、A165Cu23Fel2中三种金属的化合价均可视作零 |
| C、A165Cu23Fel2不可用作长期浸泡在海水中的材料 |
| D、1mol A165Cu23Fel2溶于过量的硝酸时共失去265mol电子 |
 感光高分子材料是制作大规模集成电路不可缺少的材料,感光高分子在曝光时会发生二聚反应,生成不溶性的交联高分子硬化膜,未感光部分可用溶剂或其它药品洗去.常用的感光高分子有聚肉桂酸乙烯酯,它的结构简式如右图,它感光后形成二聚交联高分子.请据此回答下列问题:
感光高分子材料是制作大规模集成电路不可缺少的材料,感光高分子在曝光时会发生二聚反应,生成不溶性的交联高分子硬化膜,未感光部分可用溶剂或其它药品洗去.常用的感光高分子有聚肉桂酸乙烯酯,它的结构简式如右图,它感光后形成二聚交联高分子.请据此回答下列问题: 和
和 外还有两种,请写出其结构简式:
外还有两种,请写出其结构简式: