题目内容
15.在标准状况下,35.5g氯气的体积是11.2L,将其与氢气完全化合需氢气的物质的量是0.5mol,将生成的气体配制成1L溶液,溶质的物质的量浓度是1mol•L-1.分析 标况下,气体摩尔体积是22.4L/mol,根据V=$\frac{m}{M}{V}_{m}$计算氯气体积,氯气和氢气反应方程式为Cl2+H2$\frac{\underline{\;点燃\;}}{\;}$2HCl,根据氯气和氢气之间关系式计算需要氢气物质的量;根据Cl原子守恒计算生成n(HCl),由c=$\frac{n}{V}$计算盐酸浓度.
解答 解:标况下,气体摩尔体积是22.4L/mol,(Cl2)=$\frac{35.5g}{71g/mol}$=0.5mol,
V(Cl2)=nVm=$\frac{m}{M}{V}_{m}$=$\frac{35.5g}{71g/mol}$×22.4L/mol=11.2L,氯气和氢气反应方程式为Cl2+H2$\frac{\underline{\;点燃\;}}{\;}$2HCl,根据氯气和氢气之间关系式得需要n(H2)=n(Cl2)=0.5mol;根据Cl原子守恒计算生成n(HCl)=2n(Cl2)=1mol,c(HCl)=$\frac{n}{V}$=$\frac{1mol}{1L}$=1mol/L,
故答案为:11.2;0.5;1.
点评 本题考查物质的量有关计算,为高频考点,明确各个物理量关系是解本题关键,熟练掌握物质的量基本公式并灵活运用,题目难度不大.

练习册系列答案
相关题目
20.化学与人类生活密切相关.关于下列物质的使用不合理的是( )
| A. | 单质硅可用于制造光纤制品 | B. | 碳酸氢钠常用于焙制糕点 | ||
| C. | 氧化铝可用于制造耐火坩埚 | D. | 氢氧化铝常用于治疗胃酸过多 |
7.纯碱和小苏打是厨房中两种常见的用品,它们都是白色固体.下列区分这两种物质的方法正确的是( )
| A. | 等质量的碳酸钠和碳酸氢钠分别与足量的盐酸反应,前者产生二氧化碳少 | |
| B. | 用洁净铁丝蘸取两种样品在酒精灯火焰上灼烧,火焰颜色呈黄色的是小苏打 | |
| C. | 分别用炒锅加热两种样品,全部分解挥发,没有残留物的是小苏打 | |
| D. | 先将两样品配成溶液,后分别加入石灰水,无白色沉淀生成的是小苏打 |
4.下列化学用语使用正确的组合是( )
①氘表示为12D
②乙炔的分子结构模型示意图:
③有机还原剂LiAlH4中,氢显-1价
④质量为40的钙原子:4020Ca
⑤NH4Cl的电子式: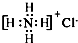
⑥2-甲基丁醇的结构简式: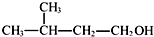
①氘表示为12D
②乙炔的分子结构模型示意图:

③有机还原剂LiAlH4中,氢显-1价
④质量为40的钙原子:4020Ca
⑤NH4Cl的电子式:
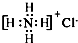
⑥2-甲基丁醇的结构简式:
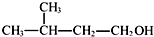
| A. | ①②③ | B. | ③④ | C. | ②④⑤ | D. | ①④⑥ |
5.分子式为C5H12O的醇与C4H8O2的羧酸在浓H2SO4存在时共热生成的酯有( )
| A. | 6种 | B. | 16种 | C. | 32种 | D. | 12种 |
