题目内容
15.在一定条件下,Na2CO3溶液中存在水解平衡:CO32-+H2O?HCO3-+OH-.下列说法不正确的是( )| A. | 通入CO2,溶液pH减小 | |
| B. | 加入少量NH4Cl固体,平衡向正反应方向移动 | |
| C. | 慢慢升高温度,$\frac{c(HC{O}_{3}^{-})}{c(C{O}_{3}^{2-})}$逐渐减小 | |
| D. | 加入NaOH 固体后冷却到室温,溶液的KW=c(OH-)•c(H+)不变 |
分析 根据平衡常数与温度的关系及温度、浓度对平衡的影响来分析解答;
A、碳酸钠溶液中通入CO2会发生反应生成碳酸氢钠;
B、加入氯化铵固体,根据铵根离子水解显示酸性来确定平衡的移动方向;
C、水解平衡是吸热的,升高温度,水解平衡正向移动,根据移动方向确定离子浓度的变化;
D、水的离子积是温度的常数,温度不变,水的离子积不变化.
解答 解:A、碳酸钠溶液中通入CO2会发生反应生成碳酸氢钠,实质是二氧化碳消耗氢氧根离子,促使平衡正向移动,所以碱性减弱,溶液pH减小,故A正确;
B、加入氯化铵固体,根据铵根离子水解显示酸性,消耗氢氧根离子,平衡正向移动,故B正确;
C、水解平衡是吸热的,升高温度,水解平衡正向移动,碳酸氢根离子浓度增加,碳酸根离子浓度减小,比值变大,故C错误;
D、水的离子积是温度的常数,加入NaOH 固体,温度不变,水的离子积KW不变化,故D正确.
故选C.
点评 本题考查水解平衡常数及影响水解平衡的因素,难度不大,水解平衡常数和化学平衡常数一样是温度的函数,与条件无关.化学平衡移动原理同样适合水解平衡的移动,要多迁移,多联系.

练习册系列答案
相关题目
5.水溶液中能大量共存的一组离子是( )
| A. | NH4+、Ba2+、Brˉ、CO32ˉ | B. | Clˉ、NO3ˉ、Fe2+、H+ | ||
| C. | K+、Na+、SO42ˉ、MnO4ˉ | D. | Na+、H+、SO42ˉ、HCO3ˉ |
6.某化合物的结构图1(键线式)及球棍模型如图2:

该有机分子的核磁共振氢谱图如图3(单位是ppm).下列关于该有机物的叙述,不正确的是( )

该有机分子的核磁共振氢谱图如图3(单位是ppm).下列关于该有机物的叙述,不正确的是( )
| A. | 该有机物不同化学环境的氢原子有8种 | |
| B. | 该有机物属于芳香族化合物 | |
| C. | 键线式中的Et代表的基团为-CH2CH3 | |
| D. | 1mol该有机物完全燃烧可以产生6mol水 |
10.下列物质只含有非极性键的是( )
| A. | H2O | B. | HCl | C. | NaOH | D. | O2 |
20.下列除杂操作可行的是( )
| A. | 通过浓硫酸除去HCl中的H2O | |
| B. | 通过灼热的CuO除去H2中的CO | |
| C. | 通过灼热的镁粉除去CO2中的N2 | |
| D. | 通过饱和碳酸氢钠溶液除去Cl2中的HCl |
7.下列说法正确的是( )
| A. | 焰色反应属于化学变化 | |
| B. | 酸性氧化物都是非金属氧化物 | |
| C. | 硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 | |
| D. | Na2O2不是碱性氧化物 |
4.合金材料在工农生产、国防建设中具有极其重要的用途.
(1)合金中至少有一种金属(填“金属”或“非金属”)元素,目前使用量最大的合金是钢合金,取5.6g碳素钢与足量的稀盐酸充分反应后,生成的氢气在标准状况下的体积小于2.24L(填“>”、“<”或“=”).
(2)合金可用几种不同的合适的材料在熔融状态下混合而成,钛能形成多种类型的合金,下表所示是几种金属的熔、沸点,其中不能形成相应合金的是B.
A.Ti和Al B.Ti和Na C.Ti和Ni DTi和Sn
(3)古代的炼金术士们认为通过炼制可将某些廉价的金属转化为贵重金属银或金,并在实际操作中得到了貌似黄金的“药金”.操作方法是将炉甘石(ZnCO3)、赤铜(Cu2O)和木炭混合加热.相关反应为ZnCO3$\frac{\underline{\;\;△\;\;}}{\;}$ZnO+CO2↑、2ZnO+C$\frac{\underline{\;\;△\;\;}}{\;}$2Zn+CO2↑、2Cu2O+C$\frac{\underline{\;△\;}}{\;}$4Cu+CO2↑
(4)“药金”就是现在人们所说的黄铜,不少骗子常利用其颜色与黄金相似的特点将其冒充为“金元宝”,请你设计一种简单的方法判定某“金元宝”是假的:取少量样品浸入稀盐酸中(或稀硫酸),若有气体产生,则该样品为假黄金;若没有气体产生,则样品为黄金.
(1)合金中至少有一种金属(填“金属”或“非金属”)元素,目前使用量最大的合金是钢合金,取5.6g碳素钢与足量的稀盐酸充分反应后,生成的氢气在标准状况下的体积小于2.24L(填“>”、“<”或“=”).
(2)合金可用几种不同的合适的材料在熔融状态下混合而成,钛能形成多种类型的合金,下表所示是几种金属的熔、沸点,其中不能形成相应合金的是B.
| Na | Ni | Al | Ti | Sn | |
| 熔点(℃) | 97.5 | 1453 | 660 | 1660 | 231.9 |
| 沸点(℃) | 883 | 2732 | 2200 | 3287 | 2270 |
(3)古代的炼金术士们认为通过炼制可将某些廉价的金属转化为贵重金属银或金,并在实际操作中得到了貌似黄金的“药金”.操作方法是将炉甘石(ZnCO3)、赤铜(Cu2O)和木炭混合加热.相关反应为ZnCO3$\frac{\underline{\;\;△\;\;}}{\;}$ZnO+CO2↑、2ZnO+C$\frac{\underline{\;\;△\;\;}}{\;}$2Zn+CO2↑、2Cu2O+C$\frac{\underline{\;△\;}}{\;}$4Cu+CO2↑
(4)“药金”就是现在人们所说的黄铜,不少骗子常利用其颜色与黄金相似的特点将其冒充为“金元宝”,请你设计一种简单的方法判定某“金元宝”是假的:取少量样品浸入稀盐酸中(或稀硫酸),若有气体产生,则该样品为假黄金;若没有气体产生,则样品为黄金.
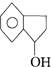 互为同分异构,满足下列三个条件:
互为同分异构,满足下列三个条件: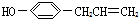
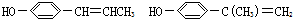 (其中两个).
(其中两个).