题目内容
物质的量是高中化学中常用的物理量,请完成以下有关其内容的计算:
(1)标准状况下,含有相同氧原子数的CO与CO2的体积之比为 .
(2)等温等压下,等体积的O2和O3所含分子个数比为 ,原子个数比为 ,质量比为 .
(3)设NA为阿伏加德罗常数的数值,如果a g某气中含有的分子数为b,则c g某气在标准状况下的体积约是 . (用含NA的式子表示).
(4)配制100mL 1mol?L-1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为,1.84g?mL-1,质量分数为98%)的体积为 mL.
(5)100mL 某Al2(SO4)3溶液中,n(Al3+)=0.20mol,则其中c(SO42-)= mol/L.
(6)某氯化镁溶液的密度为1.18g/cm3,其中镁离子的质量分数5.6%,300mL该溶液中Cl-的物质的量等于 .
(1)标准状况下,含有相同氧原子数的CO与CO2的体积之比为
(2)等温等压下,等体积的O2和O3所含分子个数比为
(3)设NA为阿伏加德罗常数的数值,如果a g某气中含有的分子数为b,则c g某气在标准状况下的体积约是
(4)配制100mL 1mol?L-1的稀H2SO4溶液,需要用量筒量取浓H2SO4(密度为,1.84g?mL-1,质量分数为98%)的体积为
(5)100mL 某Al2(SO4)3溶液中,n(Al3+)=0.20mol,则其中c(SO42-)=
(6)某氯化镁溶液的密度为1.18g/cm3,其中镁离子的质量分数5.6%,300mL该溶液中Cl-的物质的量等于
考点:物质的量的相关计算
专题:
分析:(1)相同氧原子数,n(O)相同,以此计算CO与CO2的物质的量关系,相同条件下,物质的量之比等于体积之比;
(2)等温等压下,分子数目之比等于气体体积之比,还等于物质的量比;根据物质的量之间的关系求出质量关系;
(3)先求出ag气体含有的分子数,再求出其物质的量,最后根据气体体积公式求出体积;
(4)根据c=
计算浓硫酸的物质的量浓度,再根据溶液稀释前后物质的量不变计算所需浓硫酸的体积;
(5)Al2(SO4)3溶液,阳离子、阴离子的个数之比为2:3;
(6)先根据氯化镁溶液的密度及镁离子的质量分数计算出镁离子的物质的量浓度,再计算出氯离子的浓度,最后计算出300mL该溶液中含有的氯离子的物质的量.
(2)等温等压下,分子数目之比等于气体体积之比,还等于物质的量比;根据物质的量之间的关系求出质量关系;
(3)先求出ag气体含有的分子数,再求出其物质的量,最后根据气体体积公式求出体积;
(4)根据c=
| 1000ρω |
| M |
(5)Al2(SO4)3溶液,阳离子、阴离子的个数之比为2:3;
(6)先根据氯化镁溶液的密度及镁离子的质量分数计算出镁离子的物质的量浓度,再计算出氯离子的浓度,最后计算出300mL该溶液中含有的氯离子的物质的量.
解答:
解:(1)相同氧原子数,n(O)相同,CO与CO2的物质的量比为2:1,相同条件下,物质的量之比等于体积之比,所以体积之比为2:1,
故答案为:2:1;
(2)等温等压下,等体积的O2和O3所含分子个数比为1:1,则物质的量之比为1:1,所以O原子数之比为2:3;根据m=
M知,其质量之比等于其摩尔质量之比=32g/mol:48g/mol=2:3;
故答案为:1:1;2:3;2:3;
(3)根据其组分相同,所以其质量与分子数成正比,ag气体含有的分子数为:b个,质量与分子数的比列式为:ag:b个=cg:x个,
x=
个;
cg该混合气体含有的物质的量为:n=
mol,其体积为:V=n×Vm =
mol×Vm =
L
故答案为:
L;
(4)浓H2SO4的物质的量浓度c=
mol/L=18.4mol/L.根据稀释定律,稀释前后溶质的物质的量不变,来计算浓硫酸的体积,设浓硫酸的体积为xmL,所以xmL×18.4mol/L=100mL×1mol/L,解得:x≈5.4.
故答案为:5.4;
(5)Al2(SO4)3溶液,阳离子、阴离子的个数之比为2:3,c(Al3+)=
=2.0mol/L,则其中c(SO42-)=2.0mol/L×
=3.0mol/L,
故答案为:3.0;
(6)1L该氯化镁溶液中镁离子的物质的量为:n(Mg2+)=
≈2.75mol,镁离子的物质的量浓度为:2.75mol/L,
根据氯化镁的化学式可知,氯离子的浓度为:c(Cl-)=2c(Mg2+)=5.50mol/L,
300mL该氯化镁溶液中含有氯离子的物质的量为:n(Cl-)=5.50mol/L×0.3mol=1.65mol,
故答案为:1.65mol.
故答案为:2:1;
(2)等温等压下,等体积的O2和O3所含分子个数比为1:1,则物质的量之比为1:1,所以O原子数之比为2:3;根据m=
| V |
| Vm |
故答案为:1:1;2:3;2:3;
(3)根据其组分相同,所以其质量与分子数成正比,ag气体含有的分子数为:b个,质量与分子数的比列式为:ag:b个=cg:x个,
x=
| bc |
| a |
cg该混合气体含有的物质的量为:n=
| bc |
| a?NA |
| bc |
| aNA |
| 22.4bc |
| a?NA |
故答案为:
| 22.4bc |
| a?NA |
(4)浓H2SO4的物质的量浓度c=
| 1000×1.84×98% |
| 98 |
故答案为:5.4;
(5)Al2(SO4)3溶液,阳离子、阴离子的个数之比为2:3,c(Al3+)=
| 0.2mol |
| 0.1L |
| 3 |
| 2 |
故答案为:3.0;
(6)1L该氯化镁溶液中镁离子的物质的量为:n(Mg2+)=
| 1000mL×1.18g/cm3×5.6% |
| 24g/mol |
根据氯化镁的化学式可知,氯离子的浓度为:c(Cl-)=2c(Mg2+)=5.50mol/L,
300mL该氯化镁溶液中含有氯离子的物质的量为:n(Cl-)=5.50mol/L×0.3mol=1.65mol,
故答案为:1.65mol.
点评:本题考查物质的量的计算,把握质量与物质的量的关系、物质的构成及发生的化学反应为解答的关键,注重基础知识的考查,题目难度中等.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
下列关于反应热的说法正确的是( )
| A、当△H为负值时,表示该反应为吸热反应 |
| B、燃烧不一定是放热反应 |
| C、反应热的大小与反应物所具有的能量和生成物具有的能量无关 |
| D、反应热的大小只与反应体系的始态和终态有关 |
以下是几种常用基本物理量的名称与符号的对应关系,其中不正确的是( )
| A、物质的量--mol |
| B、质量--m |
| C、时间--t |
| D、电流--I |
无土栽培中,需配制一种含 50mol NH4Cl、16mol KCl 和24mol K2SO4的营养液.若用 KCl、NH4Cl 和 (NH4)2SO4 三种固体为原料来配制,其物质的量分别为( )
| A、2 mol、64 mol、24 mol |
| B、64 mol、2 mol、24 mol |
| C、32 mol、50 mol、12 mol |
| D、16 mol、50 mol、24 mol |
下列关于各物质的化学用语表达正确的是( )
A、四氯化碳的电子式: |
B、丙烷分子的比例模型: |
C、环己烷的结构简式: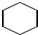 |
| D、乙酸的分子式:CH3COOH |
双酚 A是一种重要的化工原料,它的一种合成路线如图所示:
A是一种重要的化工原料,它的一种合成路线如图所示:
下列说法正确的是( )
 A是一种重要的化工原料,它的一种合成路线如图所示:
A是一种重要的化工原料,它的一种合成路线如图所示:下列说法正确的是( )

| A、1mol双酚A最多可与2mol Br2反应 |
| B、G物质是乙醛的同系物 |
| C、E物质的名称是1-溴丙烷 |
D、反应③的化学方程式是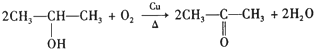 |
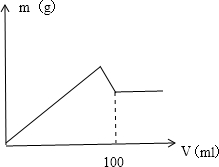 有AlCl3和MgCl2的固体混合物,取一定量的该混合物加水溶解配成溶液,实验测知Cl-的物质的量为0.70摩尔,如向该混合溶液中逐滴加入8.00mol/L的氢氧化钠溶液(密度为1.27g/ml),加入氢氧化钠溶液的体积(V)和沉淀的质量(m)有如图所示的关系.
有AlCl3和MgCl2的固体混合物,取一定量的该混合物加水溶解配成溶液,实验测知Cl-的物质的量为0.70摩尔,如向该混合溶液中逐滴加入8.00mol/L的氢氧化钠溶液(密度为1.27g/ml),加入氢氧化钠溶液的体积(V)和沉淀的质量(m)有如图所示的关系.