题目内容
12.请写出以甲苯和乙醇为原料制备化合物苯乙酸乙酯的合成路线流程图(无机试剂任选).合成路线流程图示例如下:H2C═CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.
分析 甲苯与Br2发生取代反应生成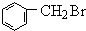 ,与NaCN发生取代反应生成
,与NaCN发生取代反应生成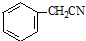 ,再根据①NaOH/②HCl得到
,再根据①NaOH/②HCl得到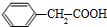 ,最后与乙醇发生酯化反应得到
,最后与乙醇发生酯化反应得到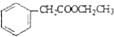 ,据此进行分析.
,据此进行分析.
解答 解:甲苯与Br2在光照的条件下发生取代反应生成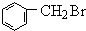 ,与NaCN发生取代反应生成
,与NaCN发生取代反应生成 ,再根据①NaOH/②HCl得到
,再根据①NaOH/②HCl得到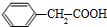 ,最后与乙醇发生酯化反应得到
,最后与乙醇发生酯化反应得到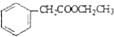 ,合成路线流程图为
,合成路线流程图为 ,
,
故答案为: .
.
点评 本题考查有机物合成,需要学生对给予的信息进行利用,是常见题型,侧重考查学生的分析推理能力,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
3.海带提碘实验中,不会用到的装置是( )
| A. | 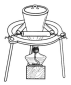 | B. |  | C. | 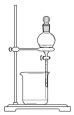 | D. | 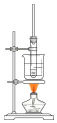 |
20.在元素周期表中,在金属元素与非金属元素的分界线附近可以找到( )
| A. | 作为催化剂的材料 | B. | 电子工业上的半导体材料 | ||
| C. | 制造农药的材料 | D. | 制造耐高温材料 |
7.钓鱼诸岛自古以来就是中国的领土,该岛附近蕴藏着大量石油和天然气.下列关于石油及石油炼制的叙述中,错误的是( )
| A. | 石油主要含碳、氢元素,是烷烃、环烷烃、芳香烃的混合物 | |
| B. | 石油中含有C5~C11的烷烃,可以通过石油的常压分馏得到汽油 | |
| C. | 含C20以上烷烃的重油经减压分馏可以得到煤油和柴油 | |
| D. | 石油经分馏得到的各馏分仍是多种烃的混合物 |
17.下列实验的反应原理用离子方程式表示正确的是( )
| A. | 用氢氧化钠溶液除去镁粉中的杂质铝:2Al+2OH-+2H2O=2AlO2-+3H2↑ | |
| B. | 室温下,测得氯化铵溶液pH<7:NH4++H2O=NH3•H2O+H+ | |
| C. | 石灰水中加入过量碳酸氢钠溶液:HCO3-+Ca2++OH-=CaCO3↓+H2O | |
| D. | 用小苏打片治疗胃酸过多:CO32-+2H+═CO2↑+H2O |
4.有些科学家提出硅是“21世纪的能源”,下列关于硅及其化合物的说法正确的是( )
| A. | 石英坩埚耐高温,可用来加热熔化烧碱、纯碱等固体 | |
| B. | 高纯度的硅单质广泛用于制作光导纤维 | |
| C. | 水泥、玻璃、水晶饰物都是硅酸盐制品 | |
| D. | 陶瓷是人类应用很早的硅酸盐材料 |
5.如表是元素周期表的一部分,表中所列的字母分别代表某一化学元素
(1)表中所列元素中属于主族元素的有a、b、c、d、f、g、h、i、j、k、l;属于金属元素的有b、c、d、e、f、h;e在元素周期表中的位置是第四周期 VIII族.
(2)下列AC组元素的单质可能都是电的良导体.
A.d、e、f B.b、c、i C.c、d、g D.a、g、k
(3)表中某元素的最高价氧化物对应水化物呈两性的化学式是Al(OH)3,
它与短周期元素b的最高价氧化物对应水化物发生反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O;
(4)b、a与j形成原子个数比为1:1:1的化合物中含有的化学键类型是离子键和共价键.
| a | ||||||||||||||||||
| g | j | |||||||||||||||||
| b | c | f | i | l | m | |||||||||||||
| e | h | k | ||||||||||||||||
(2)下列AC组元素的单质可能都是电的良导体.
A.d、e、f B.b、c、i C.c、d、g D.a、g、k
(3)表中某元素的最高价氧化物对应水化物呈两性的化学式是Al(OH)3,
它与短周期元素b的最高价氧化物对应水化物发生反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O;
(4)b、a与j形成原子个数比为1:1:1的化合物中含有的化学键类型是离子键和共价键.
6.下列反应的离子方程式书写正确的是( )
| A. | 铁粉与稀H2SO4反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | Na2CO3溶液与足量盐酸反应:CO32-+2H+═CO2↑+H2O | |
| C. | Cu(OH)2固体与稀硫酸反应:OH-+H+═H2O | |
| D. | 铝片与NaOH溶液反应:Al+OH-+H2O═AlO2-+H2↑ |