题目内容
3.在反应6HCl(浓)+KClO3═3Cl2↑+KCl+3H2O中,还原剂是HCl;若消耗 0.1mol 氧化剂,则被氧化的还原剂的物质的量是0.5mol.分析 6HCl+KClO3=KCl+3Cl2+3H2O中,Cl元素的化合价由+5价降低为0,Cl元素的化合价由-1价升高为0,以此来解答.
解答 解:6HCl+KClO3=KCl+3Cl2+3H2O中,Cl元素的化合价由+5价降低为0,Cl元素的化合价由-1价升高为0,则氧化剂为KClO3,还原剂为HCl,且6molHCl中只有5mol作还原剂,可知氧化剂和还原剂的物质的量之比为1:5,所以消耗 0.1mol 氧化剂,则被氧化的还原剂的物质的量是0.5mol,
故答案为:HCl;0.5.
点评 本题考查氧化还原反应及计算,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意部分HCl作酸,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.下列物质中,能用铝制容器贮运的是( )
| A. | 冷的稀盐酸 | B. | 冷的浓硫酸 | C. | 冷的稀硫酸 | D. | 冷的稀醋酸 |
18.下列物质中,不与水发生反应的是( )
| A. | CaO | B. | SiO2 | C. | CO2 | D. | SO2 |
15.NaCl是重要的化工原料,可以制备一系列物质.有关下列流程的说法中,正确的是( )

| A. | NaHCO3的热稳定性好 | |
| B. | 如图所示转化涉及的反应都是氧化还原反应 | |
| C. | 常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 | |
| D. | 石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 |
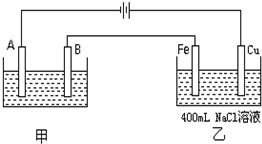 如图为相互串联的甲、乙两个电解池.试回答:
如图为相互串联的甲、乙两个电解池.试回答: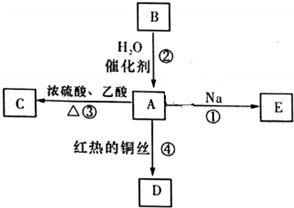 A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,能进行如图所示的多种反应.
A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,能进行如图所示的多种反应. .
.