题目内容
1.实验室用锌粒与2mol•L-1硫酸溶液制取氢气,下列措施能增大氢气产生速率的是( )| A. | 将稀硫酸改成浓硫酸 | B. | 滴加少量硫酸钠溶液 | ||
| C. | 硫酸改成4 mol•L-1的醋酸 | D. | 滴加几滴硫酸铜溶液 |
分析 A、金属锌和浓硫酸之间反应不会产生氢气;
B、滴加少量硫酸钠溶液,相当于该硫酸溶液中加入水,硫酸的浓度减少;
C、硫酸改成4 mol•L-1的醋酸,氢离子浓度增加;
D、滴加几滴硫酸铜溶液,金属锌会置换出金属铜,形成锌、铜、硫酸原电池.
解答 解:A、将稀硫酸改成浓硫酸,金属锌和浓硫酸之间反应不会产生氢气,故A错误;
B、滴加少量硫酸钠溶液,相当于该硫酸溶液中加入水,硫酸的浓度减少,因减少反应物的浓度,反应速率减慢,故B错误;
C、硫酸改成4 mol•L-1的醋酸,氢离子浓度增加,所以速率加快,故C正确;
D、滴加几滴硫酸铜溶液,金属锌会置换出金属铜,形成锌、铜、硫酸原电池,加快反应速率,故D正确.
故选CD.
点评 本题较简单,考查影响化学反应速率的常见因素如:温度、浓度、构成原电池、增大接触面等,但浓硫酸的性质是学生解答中容易忽略的知识.浓硫酸与金属反应得不到氢气.

练习册系列答案
 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
10.下列反应的离子方程式的书写不正确的是( )
| A. | 向漂粉精溶液中通入过量的二氧化碳:ClO-+H2O+CO2═HClO+HCO3- | |
| B. | 氯气与水反应:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 二氧化锰与浓盐酸反应:MnO2+4H++4Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+2Cl2↑, | |
| D. | 碳酸钙粉末与新制氯水反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
12.如图为某化学兴趣小组设计的一个原电池,装置中电流表的指针发生偏转,则X应为( )
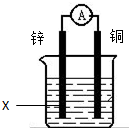

| A. | 水 | B. | 酒精 | C. | 稀硫酸 | D. | 植物油 |
9.在一定温度下的定容密闭容器中,当下列物理量不再发生变化时,表明反应A(s)+2B(g)?C(g)+D(g)已达到平衡状态的是( )
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④混合气体的平均相对分子质量
⑤气体的总物质的量.
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④混合气体的平均相对分子质量
⑤气体的总物质的量.
| A. | ②③④ | B. | ①②③ | C. | ③④⑤ | D. | ①④⑤ |
16.工业上消除氮氧化物的污染,可用如下反应:CH4(g)+2NO2(g)N2(g)+CO2(g)+2H2O(g)△H=Q kJ/mol.在温度T1和T2时,两个体积均为1 L的密闭容器中都充入1.00 mol CH4和2.40 mol NO2,测得n(CH4)随时间变化数据如下表:下列说法正确的是( )
时间/min n(CH4)/mol 温度 | 0 | 10 | 20 | 40 | 50 |
| T1 | 1.00 | 0.70 | 0.50 | 0.20 | 0.20 |
| T2 | 1.00 | 0.60 | 0.36 | … | 0.30 |
| A. | 10 min内,T1时的化学反应速率比T2时大 | |
| B. | 温度:T1<T2 | |
| C. | Q>0 | |
| D. | 化学平衡常数:K(T1)<K(T2) |
6.实验是研究化学的基础,如图装置或操作正确的是( )
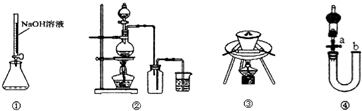

| A. | 用装置①量取15.00mL的NaOH溶液 | |
| B. | 用装置②制备并收集Cl2 | |
| C. | 用装置③陶瓷坩埚高温煅烧CaCO3固体 | |
| D. | 关闭活塞a,从b处加水,以检查装置④的气密性 |
13.甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系:甲$\stackrel{丁}{→}$乙$\stackrel{丁}{→}$丙.下列4种推断正确的是( )
①若甲为氨气,则丁可能是O2
②若丁是氢氧化钠溶液,则甲可能是一种能使品红溶液褪色的气体
③若甲为碳,则丙在一定条件下可与甲反应
④若甲为硝酸银溶液,则乙可能是一种沉淀.
①若甲为氨气,则丁可能是O2
②若丁是氢氧化钠溶液,则甲可能是一种能使品红溶液褪色的气体
③若甲为碳,则丙在一定条件下可与甲反应
④若甲为硝酸银溶液,则乙可能是一种沉淀.
| A. | ①②④ | B. | ①②③④ | C. | ①②③ | D. | ①③④ |
10.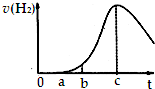 把在空气中久置的铝片5.0g投入盛有 500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图的坐标曲线来表示,则( )
把在空气中久置的铝片5.0g投入盛有 500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图的坐标曲线来表示,则( )
 把在空气中久置的铝片5.0g投入盛有 500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图的坐标曲线来表示,则( )
把在空气中久置的铝片5.0g投入盛有 500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图的坐标曲线来表示,则( )| A. | 曲线由0→a段发生了氧化还原反应 | |
| B. | 曲线由b→c段,产生氢气的速率增加较快的主要原因是反应放热 | |
| C. | c点达到了平衡 | |
| D. | c点以后,反应逐渐消耗了产生的氢气 |
11.运用铝及其化合物有关知识,回答下列问题:
(1)如图1四个图中,横坐标表示加入的物质的量,纵坐标表示生成沉淀的量,从A~D中选择符合各题要求的序号填入表
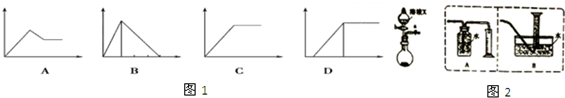
(2)测定某镁铝合金中铝含量的实验装置图如图2(夹持仪器略).
实验步骤:
步骤1:连接装置并检查装置气密性;
步骤2:称取mg镁铝合金样品置于烧瓶中,在分液漏斗中盛放足量的溶液X;
步骤3:打开分液漏斗活塞b,使反应进行,待不再产生气泡时关闭活塞b;
步骤4:待装置冷却后,调平量筒与水槽的液面,读取气体体积为xmL(折合成标准状况下干燥气体的体积).
①测定氢气体积的装置选择A(填A或B)
②为了使合金中的铝与X反应,而Mg不反应,X应选用NaOH(填化学式),反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.③计算合金中铝的质量分数为$\frac{54x}{67.2m×1{0}^{3}}$(用m,x的代数式表示).
(1)如图1四个图中,横坐标表示加入的物质的量,纵坐标表示生成沉淀的量,从A~D中选择符合各题要求的序号填入表

| 溶液 | 加入的物质 | 答案序号 |
| AlCl3溶液 | 通入过量的NH3 | ① |
| 含少量NaOH的NaAlO2溶液 | 通过量的CO2 | ② |
| NaAlO2溶液 | 滴加稀H2SO4至过量 | ③ |
| MgCl2和AlCl3的混合液 | 滴加NaOH溶液至过量 | ④ |
实验步骤:
步骤1:连接装置并检查装置气密性;
步骤2:称取mg镁铝合金样品置于烧瓶中,在分液漏斗中盛放足量的溶液X;
步骤3:打开分液漏斗活塞b,使反应进行,待不再产生气泡时关闭活塞b;
步骤4:待装置冷却后,调平量筒与水槽的液面,读取气体体积为xmL(折合成标准状况下干燥气体的体积).
①测定氢气体积的装置选择A(填A或B)
②为了使合金中的铝与X反应,而Mg不反应,X应选用NaOH(填化学式),反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.③计算合金中铝的质量分数为$\frac{54x}{67.2m×1{0}^{3}}$(用m,x的代数式表示).